
分析 (1)由N=nNA可知,分子数目之比等于其物质的量之比;氧气含有原子数目为氧气分子的2倍,臭氧分子含有氧原子数目为臭氧分子的3倍;由于氧原子质量相等,二者质量之比等于含有氧原子数目之比;O2和O3都由相同氧原子构成,二者质量相等,则含有氧原子数相等,同温同压其密度之比相对分子质量之比,以此解答该题;
(2)根据n=$\frac{V}{Vm}$计算混合气体物质的量,设CO为xmol,CO2为ymol,根据二者质量与物质的量列方程计算各自物质的量;根据M=$\frac{m}{n}$计算平均摩尔质量,进而确定平均相对分子质量.
解答 解:(1)根据m=nM,二者质量之比等于(2×48):(3×32)=1:1,即二者质量之比为1:1;
由N=nNA可知,O2和O3所含分子数之比等于其物质的量之比,即所含的分子数之比为2:3;
同温同压其密度之比相对分子质量之比,为48:32=3:2;
氧气含有原子数目为氧气分子的2倍,臭氧分子含有氧原子数目为臭氧分子的3倍,故二者含有氧原子数目之比=2×3:3×2=1:1;
根据V=nVm,得到二者的体积之比等于物质的量之比,即2:3;
故答案为:1:1;2:3;3:2;1:1;2:3;
(2)混合气体的物质的量=$\frac{6.72L}{22.4L/mol}$=0.3mol,设CO为xmol,CO2为ymol,则:x+y=0.3;28x+44y=11.6g,解得x=0.1mol,y=0.2mol,混合气体的平均摩尔质量=$\frac{11.6g}{0.3mol}$=38.7g/mol,相对分子质量在数值上和平均摩尔质量是相等的,故答案为:0.1mol;38.7.
点评 本题考查物质的量的有关计算,侧重于学生的计算能力的考查,注意把握相关计算公式列式解答该题,难度不大.


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 人们可以利用先进的化学技术和设备制造新的原子 | |
| B. | 人们可以利用催化剂使水变成汽油 | |
| C. | 人们可以利用先进的化学技术和设备制造自然界中不存在的分子 | |
| D. | 化学科学只能通过实验来探究物质的性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有② | B. | ②⑥ | C. | ①③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molFe与1molCl2充分反应,转移的电子数为3NA | |
| B. | 2L0.5mol/L亚硫酸溶液中含有的H+数为2NA | |
| C. | 60克SiO2中含有1mol SiO2分子 | |
| D. | 1L1mol•L-1的NaClO溶液中含有ClO-的数目小于1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 置换出金属铜 | B. | 产生气体,置换出金属铜 | ||
| C. | 只生成蓝色沉淀 | D. | 产生气体,生成蓝色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质熔、沸点逐渐降低 | B. | 单质的氧化性逐渐增强 | ||
| C. | 气态氢化物沸点逐渐升高 | D. | 气态氢化物稳定性逐渐减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mo1 N2和3 mol H2在一定条件下的密闭容器中充分反应,容器内的分子数2NA | |
| B. | 1 mol•L-1 FeCl3溶液中所含Cl-的数目为3NA | |
| C. | 标准状况下,22.4L14CO2与44g14CO2所含分子数均为NA | |
| D. | 标准状况下,16 g O3和O2混合气体中含有的氧原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 葡萄糖和果糖互为同分异构体,淀粉和纤维素也互为同分异构体 | |
| B. | 淀粉、油脂和蛋白质都能发生水解反应,淀粉水解的最终产物可与新制的Cu(OH)2反应 | |
| C. | 多糖、蛋白质、脂肪和聚丙烯都属于高分子化合物 | |
| D. | 汽油、柴油、植物油、棉、麻、丝、毛完全燃烧只生成CO2和H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
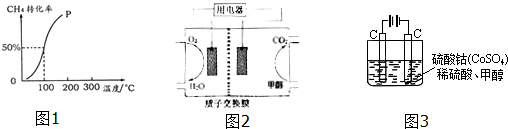
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com