
·ÖĪö ¢ŁĖįµŚŅ»²½µēĄė²śÉśµÄĖįøłŅõĄė×Ó“ųÓŠøŗµēŗÉ£¬ÓÉÓŚŅģÖÖµēŗÉĻą»„ĪüŅż£¬µŚŅ»²½²śÉśµÄH+ŅÖÖʵŚ¶ž²½µēĄė£»
¢ŚH2SeO3µÄ·Ö×Ó½į¹¹ĪŖ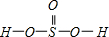 £¬SeĪŖ+4¼Ū£¬¶ųH2SeO4µÄ·Ö×Ó½į¹¹ĪŖ
£¬SeĪŖ+4¼Ū£¬¶ųH2SeO4µÄ·Ö×Ó½į¹¹ĪŖ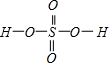 £¬SeĪŖ+6¼Ū£¬ŗóÕßSeŌ×ÓĪüµē×ÓÄÜĮ¦Ē森
£¬SeĪŖ+6¼Ū£¬ŗóÕßSeŌ×ÓĪüµē×ÓÄÜĮ¦Ē森
½ā“š ½ā£ŗ¢ŁĖįµŚŅ»²½µēĄė²śÉśµÄĖįøłŅõĄė×Ó“ųÓŠøŗµēŗÉ£¬ĪüŅżH+£¬Ķ¬Ź±²śÉśµÄH+ŅÖÖʵŚ¶ž²½µēĄė£¬ĖłŅŌH2SeO4ŗĶH2SeO3µŚŅ»²½µēĄė³Ģ¶Č“óÓŚµŚ¶ž²æµēĄė³Ģ¶Č£¬µ¼ÖĀµŚŅ»²½µēĄėŗóÉś³ÉµÄøŗĄė×Ó½ĻÄŃŌŁ½ųŅ»²½µēĄė³ö“ųÕżµēŗɵÄĒāĄė×Ó£¬
¹Ź“š°øĪŖ£ŗµŚŅ»²½²śÉśµÄH+ŅÖÖʵŚ¶ž²½µēĄė£»µŚŅ»²½µēĄėŗóÉś³ÉµÄøŗĄė×Ó½ĻÄŃŌŁ½ųŅ»²½µēĄė³ö“ųÕżµēŗɵÄĒāĄė×Ó£»
¢ŚH2SeO3µÄ·Ö×Ó½į¹¹ĪŖ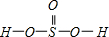 £¬SeĪŖ+4¼Ū£¬¶ųH2SeO4µÄ·Ö×Ó½į¹¹ĪŖ
£¬SeĪŖ+4¼Ū£¬¶ųH2SeO4µÄ·Ö×Ó½į¹¹ĪŖ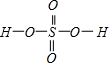 £¬SeĪŖ+6¼Ū£¬ŗóÕßSeŌ×ÓĪüµē×ÓÄÜĮ¦Ē棬µ¼ÖĀSe-O-HÖŠµÄOŌ×ÓøüĻņSeĘ«ŅĘ£¬ŌņōĒ»łÉĻĒāŌ×ÓøüČŻŅ×µēĄė³öH+£¬
£¬SeĪŖ+6¼Ū£¬ŗóÕßSeŌ×ÓĪüµē×ÓÄÜĮ¦Ē棬µ¼ÖĀSe-O-HÖŠµÄOŌ×ÓøüĻņSeĘ«ŅĘ£¬ŌņōĒ»łÉĻĒāŌ×ÓøüČŻŅ×µēĄė³öH+£¬
¹Ź“š°øĪŖ£ŗH2SeO3ŗĶH2SeO4æɱķŹ¾ĪŖ £ØHO£©SeO2ŗĶ £ØHO£©2SeO2£®H2SeO3ÖŠSeĪŖ+4¼Ū£¬¶ųH2SeO4ÖŠSeĪŖ+6¼Ū£¬ÕżµēŠŌøüøߣ¬µ¼ÖĀSe-O-HÖŠµÄOŌ×ÓøüĻņSeĘ«ŅĘ£¬Ō½Ņ×µēĄė³öH+£®
µćĘĄ ±¾Ģā×ŪŗĻæ¼²éĪļÖŹµÄ½į¹¹ÓėŠŌÖŹÖŖŹ¶£¬²ąÖŲÓŚæ¼²éѧɜµÄ·ÖĪöÄÜĮ¦ŗĶ¶Ō»ł“”ÖŖŹ¶µÄ×ŪŗĻÓ¦ÓĆÄÜĮ¦£¬ĢāÄæÄѶČÖŠµČ£¬×¢Ņā°ŃĪÕŗ¬ŃõĖįĖįŠŌĒæČõµÄÅŠ¶Ļ·½·Ø£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ļ”ĮņĖįÖŠ£ŗK+”¢MnO4-”¢CH3CH2OH | |
| B£® | pH=10µÄČÜŅŗÖŠ£ŗNa+”¢SO32-”¢NH3•H2O | |
| C£® | ÖŠŠŌČÜŅŗÖŠ£ŗNa+”¢NO3-”¢AlO2- | |
| D£® | FeCl3ČÜŅŗÖŠ£ŗH2O2”¢Mg2+”¢SO42- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 100mL pH=3µÄŃĪĖįŗĶ“×ĖįČÜŅŗ£¬Óė×ćĮæŠæ·“Ó¦£¬ĘšŹ¼Ź±¶žÕß²śÉśĒāĘųµÄĖŁĀŹ»ł±¾ĻąµČ | |
| B£® | 100mL 1mol/LµÄŃĪĖįŗĶ50mL 2mol/LµÄŃĪĖį·Ö±šÓė×ćĮæµÄŠæ·“Ó¦£¬¶žÕ߷ųöĒāĘųµÄĖŁĀŹŗĶÖŹĮæ¾łĻąµČ | |
| C£® | 100mL pH=3µÄŃĪĖįŗĶ“×ĖįČÜŅŗ£¬Óė×ćĮæŠæ·“Ó¦ŗó£¬ĖłµĆĒāĘųµÄÖŹĮæĻąµČ | |
| D£® | 100mL 0.1mol/LµÄĮņĖįŗĶŃĪĖįČÜŅŗ£¬Óė×ćĮæŠæ·“Ó¦ŗó£¬Ē°Õ߷ųöĒāĘųµÄÖŹĮæÓėŗóÕßĻąµČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
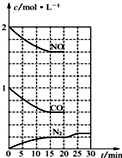 ŃŠ¾æNO2”¢SO2”¢COµČ“óĘųĪŪČ¾ĘųĢåµÄ²āĮæ¼°“¦Ąķ¾ßÓŠÖŲŅŖŅāŅ壮
ŃŠ¾æNO2”¢SO2”¢COµČ“óĘųĪŪČ¾ĘųĢåµÄ²āĮæ¼°“¦Ąķ¾ßÓŠÖŲŅŖŅāŅ壮²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ”÷H=+488.3 kJ•mol-1 | B£® | ”÷H=-244.15 kJ•mol-1 | ||
| C£® | ”÷H=-977.6 kJ•mol-1 | D£® | ”÷H=-488.3 kJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
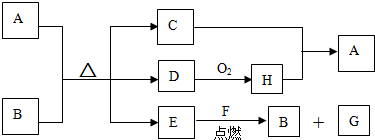
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
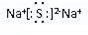 £»
£»²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com