
| A、氧化铜与稀硫酸反应:CuO+2H+═Cu2++H2O |
| B、碳酸钙和稀盐酸反应:2H++CO32-═CO2↑+H2O |
| C、氯气和氯化亚铁溶液反应:Cl2+Fe2+═Fe3++2Cl- |
| D、铜和浓硝酸反应:Cu+2H+═Cu2++H2↑ |


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、气态氢化物的热稳定性:A<C |
| B、元素A与B只能形成一种化合物 |
| C、最高价氧化物对应的水化物的酸性:C>D |
| D、原子半径的大小顺序:rB>rC>rD>rA |
查看答案和解析>>
科目:高中化学 来源: 题型:
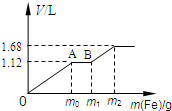 向50mL 稀H2SO4与稀HNO3的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如右图所示,且每一段只对应一个反应.下列说法正确的是( )
向50mL 稀H2SO4与稀HNO3的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如右图所示,且每一段只对应一个反应.下列说法正确的是( )| A、产生氢气的体积为1.68L |
| B、产生二氧化氮的体积为1.12L |
| C、参加反应铁粉的总质量m2=5.6g |
| D、原混合溶液中c(HNO3)=0.5 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间/min | 0 | 10 | 20 | 30 | 60 |
| pH | 4 | 3 | 2 | 1 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 现象 | 解释 |
| 钠浮在水面上 | |
| 钠熔化成光亮小球 | |
| 生成了碱性物质NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
 向一容积为1L 的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中XZ的物质的量浓度随时间变化的曲线.
向一容积为1L 的密闭容器中加入一定量的X、Y,发生化学反应aX(g)+2Y(s)?bZ(g);△H<0.如图是容器中XZ的物质的量浓度随时间变化的曲线.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com