
【题目】镁与稀硝酸的反应为:Mg+ HNO3(稀)—— Mg(NO3)2+ NO↑+ H2O
(1)配平上述化学方程式并用“双线桥法”表示该反应中电子转移的方向和数目。________
(2)该反应中,还原产物是_________,HNO3表现了______________(选填“还原性”、“氧化性”、“酸性”、“碱性”)。
(3)若反应过程中转移的电子为0.6 mol,则被还原的硝酸物质的量为________。
【答案】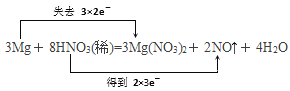 NO 氧化性,酸性 0.2 mol
NO 氧化性,酸性 0.2 mol
【解析】
(1)Mg+ HNO3(稀)—— Mg(NO3)2+ NO↑+ H2O,Mg元素的化合价由0价变成了+2价,化合价升高2,N元素的化合价由+5价变成了+2价,化合价降低3,最小公倍数是6,Mg系数为3,Mg(NO3)2系数为3,NO的系数为2,通过观察反应前后N守恒,HNO3系数为8,最后H守恒,H2O的系数为4,得出:3Mg+8HNO3(稀)=3 Mg(NO3)2+2NO↑+3H2O;用“双线桥”表示电子转移方向和数目为 ;
;
故答案为:
(2)N元素的化合价降低被还原,因此NO是还原产物,同时反应后存在NO3-,HNO3既表现氧化性,又表现酸性;
故答案为:NO;氧化性,酸性;
(3)HNO3→NO,1molHNO3被还原转移3mole-,转移0.6mol电子,则被还原的硝酸的物质的量0.2mol;
故答案为:0.2mol


 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案科目:高中化学 来源: 题型:
【题目】运用阿伏伽德罗定律及其推论,按要求填空:
(1)标准状况下,5L CH4气体与5L NH3气体的原子个数之比为______________;
(2)同温、同压下,不同体积的N2和CO气体密度之比为______________;
(3)同温、同压下,等质量的一氧化碳和二氧化碳的体积之比为______________;
(4)同温、同压下,等体积的N2和O2的质量比为________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究发现NOx和SO2是雾霾的主要成分。
I.NOx主要来源于汽车尾气,可以利用化学方法将二者转化为无毒无害的物质。
已知:N2(g)+O2(g)![]() 2NO(g) △H=+180 kJ· mol-1
2NO(g) △H=+180 kJ· mol-1
2CO(g)+O2(g)![]() 2CO2(g) △H=-564 kJ· mol-1
2CO2(g) △H=-564 kJ· mol-1
(1)2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g) △H=___________,该反应在___________下能自发进行(填“高温”低温”或“任意温度”)
2CO2(g)+N2(g) △H=___________,该反应在___________下能自发进行(填“高温”低温”或“任意温度”)
(2)T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,保持温度和体积不变,反应过程0-5min中NO的物质的量随时间变化如右图所示。
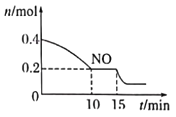
①已知:平衡时气体的分压=气体的体积分数×体系的总压强,T℃时达到平衡,此时体系的总压强为P=14MPa,则T℃时该反应的压力平衡常数Kp=___________MPa-1;平衡后,再向容器中充入NO和CO2各0.1mol,平衡将___________(填“向左”“向右”或“不")移动
②15min时,若改变外界反应条件,导致n(NO)发生如图所示的变化,则改变的条件可能是___________(填字母)
A.升温 B.增大CO浓度 C.加入催化剂 D减小容器体积
Ⅱ.SO2主要来源于煤的燃烧。燃烧烟气的脱硫减排是减少大气中含硫化合物污染的关键。
(1)已知:亚硫酸的电离常数为Ka1=2.0×10-2,Ka2=6.0×10-7。则NaSO3溶液呈___________(填“酸性”、“中性”或“碱性”)
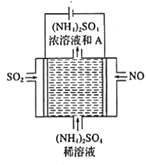
(2)如图所示的电解装置,可将雾霾中的NO、SO2转化为硫酸铵,从而实现废气的回收再利用。通入NO的电极反应式为___________;若通入的N体积为4.48L(标况下),则另外一个电极通入SO2的质量理论上应为__________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室利用下图装置用乙醇和浓硫酸反应制取乙烯,再用乙烯与溴的四氯化碳溶液反应制备1,2-二溴乙烷。
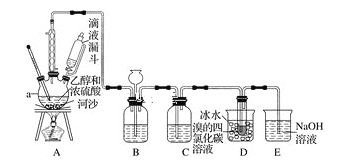
(1)在装置A中,生成的气体除乙烯外还有乙醚、CO2、SO2等,则生成乙烯的化学方程式为______________,河沙的作用是________________。仪器a的名称为________________________。
(2)装置B可起到安全瓶的作用,若气压过大,该装置中出现的现象为___________。
(3)装置C可除去CO2、SO2,所盛放的溶液为________________________。
(4)装置D中进行的主要反应的化学方程式为____________________________;把试管置于盛有冰水的小烧杯中的目的是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学用语或名称表述不正确的是( )
A.葡萄糖的分子式:C6H12O6
B.HCl的电子式:![]()
C. 的名称:2﹣甲基丙烷
的名称:2﹣甲基丙烷
D.含有10个中子的氧原子可表示为:![]() O
O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将CH4设计成燃料电池,其利用率更高,装置示意如图(A、B为多孔性碳棒)持续通入甲烷,在标准状况下,消耗甲烷体积VL。则下列说法错误的是( )

A.通入CH4的一端为原电池的负极,通入空气的一端为原电池的正极
B.0<V≤22.4 L时,电池总反应的化学方程式为CH4+2O2+2KOH=K2CO3+3H2O
C.22.4 L<V≤44.8 L时,负极电极反应为CH4-8e-+![]() +3H2O=
+3H2O=![]()
D.V=33.6 L时,溶液中只存在阴离子![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列中心原子的杂化轨道类型和分子几何构型不正确的是
A. PCl3中P原子sp3杂化,为三角锥形
B. BCl3中B原子sp2杂化,为平面三角形
C. CS2中C原子sp杂化,为直线形
D. H2S分子中,S为sp杂化,为直线形
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气是一种重要的工业原料,液氯储存区贴有的说明卡如下:
包装 | 钢瓶 |
储运要求 | 远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪 |
泄漏处理 | NaOH、NaHSO3溶液吸收 |
下列解释事实的方程式不正确的是
A. 氯气用于自来水消毒:Cl2 + H2O![]() 2H+ + Cl-+ ClO-
2H+ + Cl-+ ClO-
B. 电解饱和食盐水制取Cl2:2Cl- +2H2O![]() 2OH-+ H2↑+Cl2↑
2OH-+ H2↑+Cl2↑
C. 浓氨水检验泄露的氯气,产生白烟:8NH3 + 3Cl2 === 6 NH4Cl + N2
D. 氯气“泄漏处理”中NaHSO3溶液的作用:HSO3-+ Cl2 + H2O === SO42-+ 3H+ + 2Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识完成题目:
(1)用单线桥表示下列反应中电子转移方向和数目:KIO3+5KI+3H2SO4═3K2SO4+3I2+3H2O_____
(2)钙元素是人体必需的常量元素,所有的细胞都需要钙元素.测定人体血液中钙元素的含量常用到如下两个反应:①CaC2O4+H2SO4=H2C204+CaSO4②2KMnO4+5H2C2O4+3H2SO4=2MnSO4+K2SO4+10CO2↑+8H2O,上述反应②的还原剂是___;若收集到44.8mL(标准状况)的CO2时,消耗氧化剂___mol,有__mol电子发生转移,相当于测出含钙元素的质量是__g。
(3)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。写出碱性条件下制高铁酸钾的离子反应方程式:_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com