
| A.①③ | B.① | C.①⑤ | D.①④ |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:单选题
| A.活性炭、SO2、Na2O2都能使品红溶液褪色,但原理不同。 |
| B.同温同压下,两份相同质量的铁粉,分别与足量的稀硫酸和稀硝酸反应,产生气体的体积不相等。 |
| C.将SO2气体通入BaCl2溶液中至饱和,未见沉淀生成,继续通入NO2则有沉淀生成。 |
| D.除FeCl2溶液中的少量FeCl3,可用加入足量铁屑过滤的方法 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| 选项 | 实验现象 | 解释 |
| A | BaCl2溶液变浑浊 | SO2与BaCl2溶液反应产生了BaSO3沉淀 |
| B | Na2S溶液变浑浊 | SO2与Na2S溶液反应产生了S单质 |
| C | KMnO4溶液褪色 | SO2具有还原性 |
| D | 品红溶液褪色 | SO2具有漂白性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
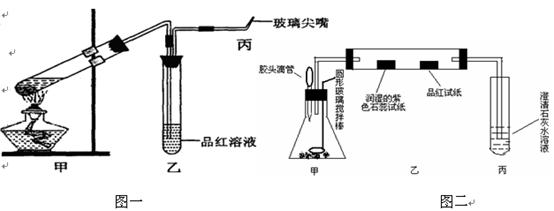
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.途径①反应中体现了浓HNO3的强氧化性和酸性 |
| B.途径②的第二步反应在实际生产中可以通过增大O2浓度来降低成本 |
| C.由途径①和②分别制取1 mol H2SO4,理论上各消耗1 mol S,各转移6 mol e- |
| D.途径②与途径①相比更能体现“绿色化学”的理念是因为途径②比途径①污染相对小且原子利用率高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.气体A为SO2和H2的混合物 | B.气体A中SO2与H2的体积比为4:1 |
| C.反应中共消耗Zn 97.5g | D.反应中共转移电子3 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

 沸点是
沸点是 )
)
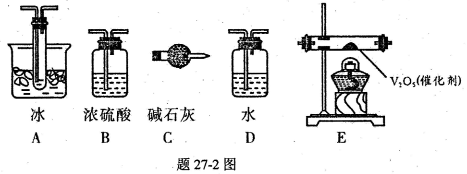
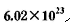 个电子转移,则该反应的化学方程式为__________________
个电子转移,则该反应的化学方程式为__________________ 粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2 —段时间后,测得装置IV增重了 mg,则实验中SO2的转化率为__________________.(用含m、n的代数式填写)
粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2 —段时间后,测得装置IV增重了 mg,则实验中SO2的转化率为__________________.(用含m、n的代数式填写)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.中性、漂白性 | B.酸性、漂白性 | C.只有酸性 | D.只有漂白性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com