
【题目】由X、Y和Z合成缓释药物M,下列说法不正确的是
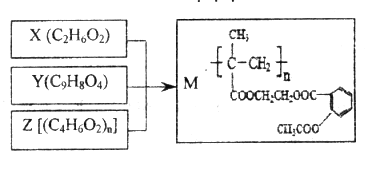
A. M在体内能缓慢发生水解反应
B. X可以由乙烯通过加成反应和取代反应制各
C. 1molY与NaOH溶液反应,最多能消耗3mol NaOH
D. Z由加聚反应制得,其单体的结构简式是CH3CH=CHCOOH
科目:高中化学 来源: 题型:
【题目】25℃时,下列各组离子在指定溶液中能大量共存的是( )
A.pH =1的溶液中:NH4+、SO42-、ClO-、Na+
B. 的溶液中:Na+、K+、MnO4-、HCO3-
的溶液中:Na+、K+、MnO4-、HCO3-
C.0.1molL-1的Na2SO3溶液中:H+、K+、SO42-、NO3-
D.澄清透明的溶液中:Fe3+、Na+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,CH3COOH和NH3·H2O的电离常数均为1.8×10-5。向20 mL浓度均为0.1 mol/L NaOH和NH3·H2O的混合液中滴加等物质的量浓度的CH3COOH溶液,所得混合液的导电率与加入CH3COOH溶液的体积(V)的关系如图所示。下列说法不正确的是

A. a=20,b=40,且溶液呈中性处于A、B两点之间
B. B点溶液中:c(CH3COO-)>c(Na+)>c(NH![]() )
)
C. 已知lg3≈0.5,则C点的pH≈5
D. A、B、C三点中,B点溶液中水的电离程度最大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】酸、碱、盐都属于电解质,是工业生产、科研领域的重要原料,请按要求回答下列问题:
(1)现有四种稀溶液,分别是:A.硫酸溶液 B.甲酸溶液 C. NaOH溶液 D.氨水
取其中两种溶液发生中和反应,请选择合适的对象完成题目的解答:
①A和C的稀溶液发生中和反应生成1mol水时,放出57.3kJ的热量,请写出此中和反应的热化学方程式______________________________.
②酸碱中和滴定时,须选择合适的指示剂,下列酸碱组合进行滴定时,不能选择甲基橙为指示剂是____(选填字母)
a.A和C b.A和D c. B和 C d. B和D
③B中甲酸的用途之一是用于配制“缓冲溶液”(HCOOH~HCOONa)。请写出甲酸电离方程式___________________________;已知一定温度下,甲酸的电离平衡常数 Ka=1.8×10-4,若用 0.2mol·L-1HCOOH 溶液100mL配制pH为4的缓冲溶液,需加入_______mL(答案保留一位小数) 0.2mol· L-1NaOH溶液。
(2)砷(As)是一些工厂和矿山废水中的污染元素,H3AsO3(亚砷酸)和H3AsO4(亚砷酸)水溶液中含砷的各物种的分布分数(平衡时某物种的浓度占各物种浓度总和的比值)与pH关系分别如图所:

①以酚酞为指示剂,将NaOH溶液逐滴加入到H3AsO3溶液中,当溶液由无色变为浅红色时停止滴加,此时砷元素的主要存在形式为________________(填微粒的化学式)②已知 pKa1 = —lgKa1
H3AsO4第一步电离方程式为H3AsO4![]() H2AsO4- + H+ 电离常数为Ka1,则pKa1=______。
H2AsO4- + H+ 电离常数为Ka1,则pKa1=______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一些常见有机物的转化如图下列说法正确的是( )

A. 上述有机物中只有C6H12O6属于糖类物质 B. 物质A和B都属于电解质
C. 物质C和油脂类物质互为同系物 D. 转化1可在人体内完成,该催化剂属于蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将![]() 转变为
转变为![]() 的方法为( )
的方法为( )
A.与足量的NaOH溶液共热后,再通入CO2
B.溶液加热,通入足量的HCl
C.与稀H2SO4共热后,加入足量的Na2CO3
D.与稀H2SO4共热后,加入足量的NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,分别对反应C(s)+CO2(g)![]() 2CO(g)(ΔH>0)进行如下操作(只改变该条件):①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减少体系中CO的量。上述措施中一定能使反应速率显著变大的是
2CO(g)(ΔH>0)进行如下操作(只改变该条件):①升高反应体系的温度;②增加反应物C的用量;③缩小反应体系的体积;④减少体系中CO的量。上述措施中一定能使反应速率显著变大的是
A.①②③④B.①③④C.①②D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】低碳经济成为人们一种新的生活理念,二氧化碳的捕捉和利用是一个重要研究方向, 既可变废为宝,又可减少碳的排放。工业上可用CO2和H2制备被誉为“21世纪的清洁燃料”二甲醚(CH3OCH3):
如在500℃时,在密闭容器中将炼焦中的CO2转化为二甲醚,其相关反应为:
主反应I:2CO2 (g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) △H1
CH3OCH3(g)+3H2O(g) △H1
副反应II:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H2
CH3OH(g)+H2O(g) △H2
(1)已知:①CO(g)+2H2(g)![]() CH3OH(g) △H=-90.1kJ/mol
CH3OH(g) △H=-90.1kJ/mol
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H=-24.5kJ/mol
CH3OCH3(g)+H2O(g) △H=-24.5kJ/mol
③CO(g)+H2O(g)![]() CO2(g)+H2(g) △H= -41.0kJ/mol
CO2(g)+H2(g) △H= -41.0kJ/mol
则主反应I的△H1=______。
(2)在一定温度下某密闭容器中按CO2和H2的浓度比为1:3投料进行反应,测得不同时间段部分物质的浓度如下表:

①10-20min 内,CH3OCH3的平均反应速率v(CH3OCH3)=_______。
②根据以上数据计算主反应I的平衡常数K=______(列式,代入数据,不计算结果)。
(3)欲提高CH3OCH3产率的关键的因素是选用合适的催化剂,其原因是_______。
(4)对于反应II,温度对CO2的转化率及催化剂的效率影响如图所示:下列有关说法不正确的是_______。

A.其他条件不变,若不使用催化剂,则250℃时CO2的平衡转化率可能位于Ml
B.温度低于250°C时,随温度升高甲醇的产率增大
C.M点时平衡常数比N点时平衡常数大
D.实际反应应尽可能在较低的温度下进行,以提高CO2的转化
(5)利用太阳能电池将CO2转化为乙烯、丙烯等有机化工原料,其工作原理如图所示。则a为太阳能电池的_______极,写M极上生成丙烯的电极反应式为_________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下向10mL0.1mol/LNaOH溶液中加入0.1mol/L的一元酸HA溶液,溶液pH的变化曲线如图所下列说法不正确的是
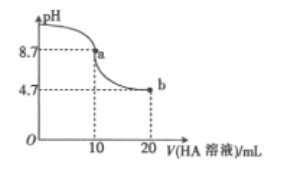
A. a点所示溶液中:c(A-)>c(Na+)>c(OH-)>c(H+)
B. a点所示溶液中:c(Na+)=0.05mol/L
C. pH=7时,c(Na+)=c(A-)
D. b点所示溶液中:c(Na+)<c(A-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com