
| A.青石棉是一种硅酸盐产品 |
| B.青石棉中含有一定量的石英晶体 |
| C.青石棉的化学组成可表示为:Na2O·3FeO·Fe2O3·8SiO2·H2O |
| D.1 mol青石棉能使1 mol HNO3被还原 |
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源:不详 题型:填空题
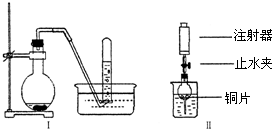
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

| 物质 | Si | SiCl4 | SiHCl3 | SiH2Cl2 | SiH3Cl | HCl | SiH4 |
| 沸点/℃ | 2355 | 57.6 | 31.8 | 8.2 | -30.4 | -84.9 | -111.9 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

| 物 质 | SiCl4 | BCl3 | AlCl3 | FeCl3 | PCl5 |
| 沸点/℃ | 57.7 | 12.8 | - | 315 | - |
| 熔点/℃ | -70.0 | -107.2 | - | - | - |
| 升华温度/℃ | - | - | 180 | 300 | 162 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用盐的形式表示:BaSiO3·CuSiO3 |
| B.用氧化物形式表示:BaO·CuO·2SiO2 |
| C.易溶于强酸、强碱 |
| D.性质稳定,不易褪色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
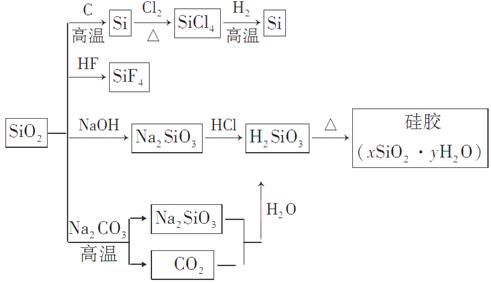
| A.SiO2属于两性氧化物 |
| B.盛放Na2CO3溶液的试剂瓶不能用玻璃塞 |
| C.硅胶吸水后不能重复再生 |
| D.图中所示转化反应都是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.利用Si和O在周期表中的位置 |
| B.SiO2与水不发生反应 |
| C.Si在一定条件下与氧气反应,生成SiO2 |
| D.H2SiO3的酸性比H2O的酸性强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 材料 | 主要化学成分 |
| A | 刚玉、金刚石 | 三氧化二铝 |
| B | 大理石、石灰石 | 碳酸钙 |
| C | 普通水泥、普通玻璃 | 硅酸盐 |
| D | 沙子、石英 | 二氧化硅 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com