
下列反应的离子方程式不正确的是()
A. 用盐酸清除水垢CaCO3+2H+=Ca2++CO2↑+H2O
B. Fe跟稀硫酸反应:Fe+2H+=Fe2++H2↑
C. 澄清石灰水跟稀盐酸:H++OH﹣=H2O
D. 碳酸氢钠溶液跟氢氧化钠溶液反应HCO3﹣+OH﹣=H2O+CO2↑
考点: 离子方程式的书写.
分析: A.碳酸钙与盐酸反应生成氯化钙、二氧化碳和水;
B.铁与稀硫酸反应生成硫酸亚铁和氢气;
C.澄清石灰水跟稀盐酸反应生成氯化钙和水;
D.碳酸氢钠溶液跟氢氧化钠溶液反应生成碳酸钠和水.
解答: 解:A.碳酸钙与盐酸反应生成氯化钙、二氧化碳和水,离子方程式为:CaCO3+2H+=Ca2++CO2↑+H2O,故A正确;
B.铁与稀硫酸反应生成硫酸亚铁和氢气,离子方程式为:Fe+2H+=Fe2++H2↑,故B正确;
C.澄清石灰水跟稀盐酸反应生成氯化钙和水,离子方程式为:H++OH﹣=H2O,故C正确;
D.碳酸氢钠溶液跟氢氧化钠溶液反应生成碳酸钠和水,离子方程式为:HCO3﹣+OH﹣=H2O+CO32﹣,故D错误;
故选:D.
点评: 本题考查离子反应的书写,为高频考点,把握发生的化学反应及离子反应的书写方法为解答的关键,注意化学式的拆分,题目难度不大.


科目:高中化学 来源: 题型:
配制一定物质的量浓度的NaOH溶液时,可造成所配溶液浓度偏高的是()
A. 所用NaOH已吸潮
B. 向容量瓶滴加水时液面低于刻度线即摇匀
C. 有少量NaOH溶液残留在烧杯内
D. 向容量瓶加水时眼睛一直仰视液面
查看答案和解析>>
科目:高中化学 来源: 题型:
反应H2(g)+I2(g)⇌2HI(g)在体积固定的密闭容器中进行,达到平衡状态的标志是()
①单位时间内断裂n mol H﹣H键的同时形成2n mol H﹣I键
②单位时间内生成n molI2的同时生成2n molHI
③2v正(H2)=v逆(HI)
④HI分子数不再改变
⑤混合气体颜色不再改变
⑥混合气体压强不再改变.
A. ②④⑤⑥ B. ②③④⑤ C. ①③④⑤ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作中数据合理的是()
A. 用10 mL 量筒量取5.2 mL盐酸
B. 用广泛pH试纸测得某溶液的pH值为12.5
C. 用托盘天平称取25.12gNaCl固体
D. 用100 mL容量瓶配制50mL0.1 mol/L的盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,既属于化合反应,又属于氧化还原反应的是()
A. H2+Cl2 2HCl B. 2H2O2
2HCl B. 2H2O2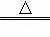 2H2O+O2↑
2H2O+O2↑
C. CaO+H2O=Ca(OH)2 D. Zn+H2SO4=ZnSO4+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
①同温、同压下,质量相等的SO2和CO2相比较,体积之比为 ,
已知SO2和CO2均为酸性氧化物,写出CO2与足量NaOH溶液反应的离子方程式 ;
②某溶液中可能含有大量下列阴离子:OH﹣、SO42﹣、CO32﹣、Cl﹣.
(1)当溶液中存在大量H+时,则溶液中不可能有 .
(2)当溶液中有大量的Ba2+存在时,则溶液中不可能有 ,用离子方程式写出不可能存在的原因 、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
已知含氧酸可用通式XOm(OH)n表示,如X是S,m=2,n=2,则这个式子表示为H2SO4.一般而言,该式中m 大的是强酸,m小的是弱酸.下列各含氧酸中酸性最强的是( )
|
| A. | HClO3 | B. | H2SeO3 | C. | H2BO2 | D. | HMnO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
关于如图所示装置的叙述,正确的是()
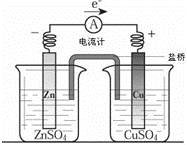
A. 铜是阳极,铜片上有气泡产生
B. 铜片质量逐渐减少
C. 电流从锌片经导线流向铜片
D. 铜离子在铜片表面被还原
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com