
| 时间(s) | 1 | 2 | 3 | 4 | |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 |
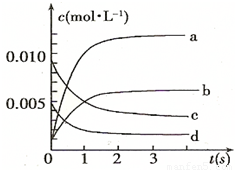
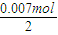 =0.0035mol/L,由方程式2NO(g)+O2(g)?2NO2(g)可知,平衡时△c(NO):△c(O2):△c(NO2)=2:1:2,据此判断表示NO2的浓度变化的曲线,
=0.0035mol/L,由方程式2NO(g)+O2(g)?2NO2(g)可知,平衡时△c(NO):△c(O2):△c(NO2)=2:1:2,据此判断表示NO2的浓度变化的曲线, 计算v(NO),再根据速率之比等于化学计量数之比计算v(O2);
计算v(NO),再根据速率之比等于化学计量数之比计算v(O2);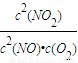 ,
,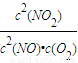 ;放热;
;放热;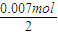 =0.0035mol/L,曲线b平衡时的浓度为0.0035mol/L,故曲线b表示NO2的浓度变化,
=0.0035mol/L,曲线b平衡时的浓度为0.0035mol/L,故曲线b表示NO2的浓度变化, =0.003mol/(L?s),根据速率之比等于化学计量数之比,故v(O2)=
=0.003mol/(L?s),根据速率之比等于化学计量数之比,故v(O2)= v(NO)=
v(NO)= ×0.003mol/(L?s)=0.0015mol/(L?s),
×0.003mol/(L?s)=0.0015mol/(L?s),

科目:高中化学 来源: 题型:
| 时间/s | 0 | 1 | 2 | 3 | 4 |
| n(A)/mol | 2.0 | 1.0 | 0.8 | 0.8 | 0.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| N2+3H2?2NH3 | ||||
| 温度 | 25℃ | 200℃ | 400℃ | 600℃ |
| 平衡常数K | 5×108 | 650 | 0.507 | 0.01 |
查看答案和解析>>
科目:高中化学 来源: 题型:
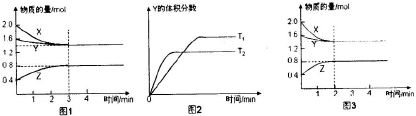
| A、反应进行的前3min内,用X表示的反应速率V(X)=0.1mol/(L?min) | B、平衡时容器内的压强为反应前的0.8倍 | C、保持其他条件不变,升高温度,反应的化学平衡常数K减小 | D、若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 时间/s | 0 | 1 | 2 | 3 | 4 |
| n(A)/mol | 2.0 | 1.0 | 0.8 | 0.8 | 0.8 |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年北京市门头沟区育园中学高二(下)期末化学试卷(解析版) 题型:填空题
| 时间/s | 1 | 2 | 3 | 4 | |
| n(A)/mol | 2.0 | 1.0 | 0.8 | 0.8 | 0.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com