
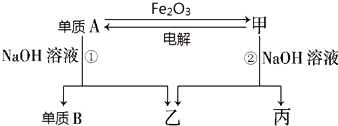
分析 单质A常作为食品包装材料,甲是两性氧化物,A与氧化铁反应得到甲,且A能与NaOH反应,则A为Al,甲为Al2O3,单质B为H2,乙为NaAlO2,丙为NaAlO2,据此解答.
解答 解:单质A常作为食品包装材料,甲是典型的两性氧化物,A与氧化铁反应得到甲,且A能与NaOH反应,则A为Al,甲为Al2O3,单质B为H2,乙为NaAlO2,丙为NaAlO2,
(1)反应①的离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(2)A为金属Al,单质A与Fe2O3反应为铝热反应,铝热反应需要引发剂引发高温反应,镁条在空气中可以燃烧,氧气是氧化剂,但插入混合物中的部分镁条燃烧时,氯酸钾则是氧化剂,以保证镁条的继续燃烧,同时放出足够的热量引发氧化铁和铝粉的反应,反应方程式为2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe,铝热反应的应用为焊接钢轨等,
故答案为:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Fe;镁粉和氯酸钾;焊接钢轨等;
(3)铝能与氢氧化钠反应生成偏铝酸钠和氢气,据此可设计一个简单的实验方案,证明铝热反应的产物中含有单质铝,具体操作为取少量块状熔融物于烧杯中,加入氢氧化钠溶液,若有气泡冒出,则证明含有单质铝,
故答案为:取少量块状熔融物于烧杯中,加入氢氧化钠溶液,若有气泡冒出,则证明含有单质铝.
点评 本题考查无机物推断,涉及Al元素化合物性质、铝热反应、金属冶炼、离子方程式书写等,难度不大,需要学生熟练掌握元素化合物性质,比较基础.


科目:高中化学 来源: 题型:选择题
| A. | 根据醋酸溶液中分子和离子共存,即可证明溶液达到了电离平衡状态 | |
| B. | c(CH3COO-)=c(H+),则醋酸溶液达到电离平衡状态 | |
| C. | 当NH3•H2O达到电离平衡时,溶液中NH3•H2O和OH-的浓度肯定相等 | |
| D. | 磷酸是分步电离的,电离程度依次减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 随着药店的普及,药物都可以直接去药店购买,不需要去医院 | |
| B. | 青霉素时一种常用药,感冒发烧、咳嗽肺炎都可以使用 | |
| C. | 长期大量使用阿司匹林可预防疾病,没有副作用 | |
| D. | 虽然药物能治病,但大部份药物有毒副作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 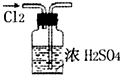 干燥Cl2 干燥Cl2 | B. | 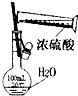 配制100ml 0.1mol•L-1硫酸溶液 | ||
| C. | 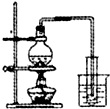 制取少量蒸馏水 | D. |  检验钾元素的存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量金属钠加到冷水中:Na+2H2O=Na++OH-+H2↑ | |
| B. | 铁粉加到盐酸中:2Fe+6H+=Fe3++3H2↑ | |
| C. | 石灰石溶解在稀HCl中:CO32-+2H+═CO2↑+H2O | |
| D. | 硫酸溶液与氢氧化钡溶液混合:Ba2++2OH-+SO42-+2H+═2H2O+BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 采用直接加热绿矾(FeSO4•xH2O)晶体的方法制备无水硫酸亚铁 | |
| B. | 用KMnO4标准溶液滴定H2C2O4溶液时,眼睛时刻关注着锥形瓶内溶液颜色变化 | |
| C. | 在中和热测定实验中,为保证稀盐酸充分反应,将氢氧化钠溶液应分少量多次加入 | |
| D. | 为测定新制氯水pH,用玻璃棒蘸取液体滴在pH试纸上,再对照标准比色卡读数 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
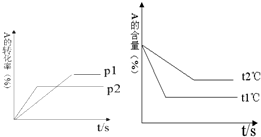 可逆反应:aA(g)+bB(g) cC(g)+dD(g);根据图回答:
可逆反应:aA(g)+bB(g) cC(g)+dD(g);根据图回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| n(HI)/mol | 0.180 | 0.164 | 0.152 | 0.144 | 0.140 | 0.140 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com