
【题目】有关物质的转化关系如下图所示(部分生成物与反应条件已略去)。其中A是最常见的无色液体,B、C、D、E均为单质,G是一种极易溶于水的碱性气体,F是胃酸的主要成分,K是不溶于稀硝酸的白色沉淀,反应4是工业制X的主要反应之一。

(1)G的电子式为_____________。
(2)I的化学式为____________。
(3)写出反应2的离子方程式________________________________________。
(4)写出反应4的化学方程式________________________________________。
【答案】![]() AgNO3 Ag+2H++NO3-=Ag++NO2↑+H2O 4NH3+5O2
AgNO3 Ag+2H++NO3-=Ag++NO2↑+H2O 4NH3+5O2![]() 4NO+6H2O
4NO+6H2O
【解析】
A是最常见的无色液体,A是水,电解水生成氢气和氧气。B、C、D、E均为单质,G是一种极易溶于水的碱性气体,G是氨气,则D是氢气,C是氧气,E是氮气,氨气催化氧化生成水和NO,J是NO。反应4是工业制X的主要反应之一,X是硝酸,则H是二氧化氮。F是胃酸的主要成分,F是氯化氢。K是不溶于稀硝酸的白色沉淀,所以B是单质银,I是硝酸银,K是氯化银,据此解答。
根据以上分析可知A是水,B是银,C是氧气,D是氢气,E是氮气,F是氯化氢,G是氨气,H是二氧化氮,I是硝酸银,J是NO,K是氯化银,X是硝酸。
(1)G是氨气,电子式为![]() 。
。
(2)I的化学式为AgNO3。
(3)反应2的离子方程式为Ag+2H++NO3-=Ag++NO2↑+H2O。
(4)反应4的化学方程式为4NH3+5O2![]() 4NO+6H2O。
4NO+6H2O。


科目:高中化学 来源: 题型:
【题目】下列说法中,在科学上没有错误的是
A.吸带过滤嘴的香烟,对人体无害
B.人工合成的具有生命活性的蛋白质—结晶牛胰岛素,是1965年我国科学家最先合成的
C.纯天然物质配成的饮料,不含任何化学物质
D.蒸馏水绝对纯净,其中不含任何分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作规范且能达到目的的是
目的 | 操作 | |
A. | 取20.00 mL盐酸 | 在50 mL酸式滴定管中装入盐酸,调整初始读数为30.00 mL后,将剩余盐酸放入锥形瓶 |
B. | 测定醋酸钠溶液pH | 用玻璃棒蘸取溶液,点在湿润的pH试纸上 |
C. | 清洗碘升华实验所用试管 | 先用酒精清洗,再用水清洗 |
D. | 配制浓度为0.010 | 称取KMnO4固体0.158 g,放入100 mL容量瓶中,加水溶解并稀释至刻度 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关有机化合物的组成、性质的说法,正确的是( )
A.水煤气、液化石油气的成分相同
B.葡萄糖、淀粉和乙酸乙酯在一定条件下都能发生水解反应
C.淀粉、蛋白质均属于高分子化合物,而油脂不属于高分子化合物
D.石油的裂解是化学变化,而石油的分馏和煤的干馏都是物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知锌与稀盐酸反应放热,某学生为了探究反应过程中的速率变化,用排水集气法收集反应放出的氢气。所用稀盐酸浓度有1.00 mol·L-1、2.00 mol·L-1两种浓度,每次实验稀盐酸的用量为25.00 mL,锌有细颗粒与粗颗粒两种规格,用量为6.50 g。实验温度为298 K、308 K。
(1)完成以下实验设计(填写表格中空白项),并在实验目的一栏中填出对应的实验编号:
编号 | T/K | 锌规格 | 盐酸浓度/mol·L-1 | 实验目的 |
① | 298 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究盐酸浓度对该反应速率的影响; (Ⅱ)实验①和_______探究温度对该反应速率的影响; (Ⅲ)实验①和______探究锌规格(粗、细)对该反应速率的影响。 |
② | 298 | 粗颗粒 | 1.00 | |
③ | 308 | 粗颗粒 | 2.00 | |
④ | 298 | 细颗粒 | 2.00 |
(2)实验①记录如下(换算成标况):
时间(s) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | span>100 |
氢气体积 (mL) | 16.8 | 39.2 | 67.2 | 224 | 420 | 492.8 | 520.8 | 543.2 | 554.4 | 560 |
①计算在30s~40s范围内盐酸的平均反应速率ν(HCl)=________(忽略溶液体积变化)。
②反应速率最大的时间段(如0s~10s......)为_______,可能原因是______。
③反应速率最小的时间段为________,可能原因是_________________________________。
(3)另一学生也做同样的实验,由于反应太快,测量氢气的体积时不好控制,他就事先在盐酸溶液中分别加入等体积的下列溶液以减慢反应速率,在不影响产生H2气体总量的情况下,你认为他上述做法中可行的是____________(填相应字母);
A.氨水 B.CuCl2溶液 C.NaCl溶液 D.KNO3溶液
(4)另有某温度时,在2L容器中X、Y、Z物质的量随时间的变化关系曲线如下图所示,该反应的化学方程式为:_____________________________。
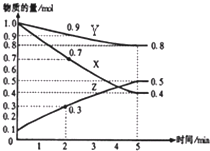
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容中发生下列反应aA(g)![]() cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.8倍,下列叙述正确的是
A. A的转化率变小 B. 平衡向正反应方向移动
C. D的体积分数变大 D. a> c+d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,某反应达平衡,平衡常数K=![]() 。恒容时,温度升高,H2浓度减小。下列说法正确的是
。恒容时,温度升高,H2浓度减小。下列说法正确的是
A、该反应的焓变为正值
B、恒温恒容下,增大压强,H2浓度一定减小
C、升高温度,逆反应速率减小
D、该反应化学方程式为CO+H2O=CO2+H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)反应m A+n B ![]() p C在某温度下达到平衡。
p C在某温度下达到平衡。
①若A、B、C都是气体,减压后正反应速率小于逆反应速率,则m、n、p的关系__________。
②若A、B、C都是气体,且m + n < p,而加压或升温平衡移动方向相同,则△H ______0
(2)将1molN2和4molH2充入容积为2L的密闭容器中发生:N2(g)+ 3H2(g) ![]() 2NH3(g) ,2分钟后反应达平衡后,N2的浓度为0.25 mol/L,完成:
2NH3(g) ,2分钟后反应达平衡后,N2的浓度为0.25 mol/L,完成:
①N2转化率是____________
②用NH3 表达的化学反应速率为:___________
③平衡常数值是________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列过程或现象与盐类水解无关的是( )
A.纯碱溶液去油污B.铁在潮湿的环境下生锈
C.加热氯化铁溶液颜色变深D.0.1 mol/L AlCl3溶液中c(Al3+)<0.1 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com