
 为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):分析 (1)氯化钡过量时,加入硫酸会产生白色沉淀;
(2)粗盐的提纯中,加入碳酸钠的作用是除去杂质离子钙离子以及过量的钡离子;
(3)Mg(OH)2、CaCO3、BaCO3会与盐酸反应,生成氯化镁、氯化钙、氯化钡等物质,会影响制得精盐的纯度;
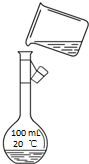
(4)图中缺少玻璃棒引流、配制150mL溶液.
解答 解:(1)在粗盐提纯时,加入过量的氯化钡的目的是除去硫酸根离子,并将之除尽,氯化钡过量时,加入硫酸会产生白色沉淀,可以通过检验钡离子来确定氯化钡是否过量,
故答案为:取上层清液,继续加BaCl2,无沉淀产生;
(2)粗盐的提纯中,加入碳酸钠的作用是除去杂质离子钙离子以及过量的钡离子,反应的方程式为:CaCl2+Na2CO3=CaCO3↓+2NaCl,BaCl2+Na2CO3=BaCO3↓+2NaCl,反应的实质是:Ca2++CO32-=CaCO3↓、Ba2++CO32-=BaCO3↓,
故答案为:Ca2++CO32-=CaCO3↓、Ba2++CO32-=BaCO3↓;
(3)若先用盐酸调pH再过滤,那样Mg(OH)2、CaCO3、BaCO3会与盐酸反应,生成易溶于水的氯化镁、氯化钙、氯化钡等物质,从而影响氯化钠的纯度,
故答案为:若过滤前加盐酸,前面所生成的沉淀会被盐酸溶液重新变为离子进入溶液;
(4)根据示意图分析,缺少玻璃棒引流,容量瓶的规格也不对,容量瓶用的是100mL应该用150mL,
故答案为:转移液体时没有用玻璃棒引流;容量瓶用的是100mL应该用150mL.
点评 本题考查了有关粗盐的提纯知识,可以根据所学知识进行回答,题目难度不大


科目:高中化学 来源: 题型:选择题

| A. | T1>T2 | |
| B. | 加入AgNO3固体,可使a点变到c点 | |
| C. | a点和b点的Ksp相等 | |
| D. | c点时,在T1、T2两个温度下均有固体析出 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100℃时Kw=10-12 | |
| B. | 加热蒸干后无任何残留物 | |
| C. | 常温100g该液体中最多溶解NaCl固体36g | |
| D. | 常温下,阳离子总浓度c=10-7mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH等于4的NH4Cl溶液 | B. | pH等于4的H2SO4溶液 | ||
| C. | pH等于10的Na2CO3溶液 | D. | 一定浓度的NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 四、IIA族,四、VIIA 族 | B. | 四、IA族,五、VIIA族 | ||
| C. | 四、IIA族,五、VIA族 | D. | 五、IA族,五、VIIA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用K37ClO3与浓盐酸制氯气:37ClO3-+6H++6Cl-═37Cl-+3Cl2↑+3H2O | |
| B. | 在溶液中等物质的量的FeBr2与Cl2反应:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| C. | 将1mol/L的NaAlO2溶液和2.5mol/L的HCl溶液等体积均匀混合 AlO2-+H++H2O═Al(OH)3↓ | |
| D. | 0.1mol/L的Na2CO3溶液中2 C(Na+)═C (HCO3-)+C (H2CO3)+C(CO32-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com