
| A. | 当电池负极消耗mg气体时,电解池阳极同时有mg气体生成 | |
| B. | 电池的正极反应式为:4OH--4e-=O2↑+2H2O | |
| C. | 电解后c(Na2CO3)不变,且溶液中有晶体析出 | |
| D. | 电池中c(KOH)不变;电解池中溶液pH变大 |
分析 该燃料电池为碱性电池,电池的正极反应为:O2+2H2O+4e-═4OH-,负极反应为:H2-2e-+2OH-═H2O,电解饱和碳酸钠溶液阴极发生的反应为:2H++2e-═H2↑,阳极反应为:4OH--4e-═O2↑+2H2O,
A.负极上氢气失电子和氢氧根离子生成水,阳极上氢氧根离子放电生成氧气,根据电子守恒计算;
B.正极上氧气得电子和水反应生成氢氧根离子;
C.电解时,阳极上氢氧根离子放电、阴极上氢离子放电,实际上是电解水,导致析出部分碳酸钠,溶液仍然是饱和溶液;
D.放电时,原电池中生成水,氢氧化钾的物质的量不变,据此确定其浓度是否变化;电解池中碳酸钠浓度不变,其pH不变.
解答 解:A.电池负极反应为:H2-2e-+2OH-═H2O,当负极消耗mg气体时,转移的电子的物质的量为 $\frac{m}{2}$mol×2=mmol,电解池阳极得电子为 m mol,阳极发生的反应为:4OH--4e-═O2↑+2H2O,阳极生成气体的质量为:$\frac{m}{4}$mol×32g/mol=8mg,故A错误;
B.该燃料电池为碱性电池,电池的正极反应为:O2+2H2O+4e-═4OH-,故B错误;
C.电解后,由于电解了水,水的质量减小,碳酸钠为饱和溶液,所以会析出碳酸钠晶体,但是仍然为碳酸钠饱和溶液,则c(Na2CO3)不变,故C正确;
D.放电时燃料电池的总反应为O2+2H2═2H2O,原电池中生成水,氢氧化钾的物质的量不变,则氢氧化钾浓度降低;电解池中碳酸钠浓度不变,其pH不变,故D错误;
故选C.
点评 本题考查了原电池原理和电解池工作原理,题目难度中等,明确电解反应实质为解答关键,注意电解后的碳酸钠溶液仍然是饱和溶液,导致其浓度、pH都不变,为易错点,试题培养了学生的分析能力及灵活应用能力..


科目:高中化学 来源: 题型:选择题
| A. | 若X为IA族时,Y不可能是第三周期VIA族元素 | |
| B. | 由X、Y、Z、W四种元素不可能形成其原子个数比为1:3:1:1的化合物 | |
| C. | Z元素的原子半径一定小于W元素的原子半径 | |
| D. | 若X为IVA族元素时,X、Y两元素可形成含有共价键的离子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在溶有1molFe(OH)3胶粒的胶体中,含有多于NA个的Fe(OH)3分子 | |
| B. | 将一束强光通过淀粉溶液,也能产生丁达尔效应 | |
| C. | “雨后彩虹”“海市蜃楼”既是一种自然现象又是光学现象,也与胶体的知识有关 | |
| D. | 纳米材料粒子直径一般从几纳米到几十纳米,因此纳米材料属于胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验编号 | c(HA)/mol•L-1) | c(NaOH)/mol•L-1 | 混合后溶液的pH |
| 甲 | 0.2 | 0.2 | pH=a |
| 乙 | b | 0.2 | pH=7 |
| 丙 | 0.2 | 0.1 | pH<7 |
| 丁 | 0.1 | 0.1 | pH=c |
| A. | 甲中:若a=7,则HA是强酸 | |
| B. | 乙中:若b≠0.2,则c(A-)=C(Na+) | |
| C. | 丙中:若HA是弱酸,则$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$<1 | |
| D. | 丁中:若 c=9,则c(OH-)-c(HA)=10-9mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
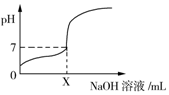 常温下,用0.1mol/L的NaOH溶液滴定20mL同浓度的一元弱酸HA,滴定过程中溶液pH随NaOH溶液体积变化曲线如图所示(忽略中和热效应),下列说法正确的是( )
常温下,用0.1mol/L的NaOH溶液滴定20mL同浓度的一元弱酸HA,滴定过程中溶液pH随NaOH溶液体积变化曲线如图所示(忽略中和热效应),下列说法正确的是( )| A. | X=20 | |
| B. | HA溶液加水稀释后,溶液中$\frac{c(HA)}{{c({A^-})}}$的值减小 | |
| C. | 0.1 mol/L的NaOH溶液中,由水电离出的c(OH-)=0.1 mol/L | |
| D. | 加入NaOH溶液体积为X mL时,溶液中c(A-)=0.05 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 泡沫灭火器中用的是苏打和硫酸铝 | |
| B. | 沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 | |
| C. | 理想的催化剂可以大幅度提高目标产物在最终产物的比率 | |
| D. | Na与H2O的反应是熵减的放热反应,该反应能自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-氯丁烷与氢氧化钠、乙醇在加热条件下的消去反应 | |
| B. | 乙烯通入溴水中的加成反应 | |
| C. | 灼热的铜丝插入足量乙醇中的氧化反应 | |
| D. | 苯酚与足量的氢气在一定条件下的加成反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com