
| A、向平衡混合物中加入少量W,正、逆反应速率均增大 |
| B、平衡后再加入1 mol X,上述反应的△H增大 |
| C、温度不变,再加入2 mol X,重新达到平衡时X的转化率大于原平衡 |
| D、当容器内混合气体的密度不变时不能证明此反应已达平衡状态 |
| m |
| V |
| m |
| V |


 一线名师提优试卷系列答案
一线名师提优试卷系列答案科目:高中化学 来源: 题型:
| A、常温下,0.01mol/LCH3COOH与pH=12的NaOH溶液混合,若混合后c(CH3COO-)>c(Na+),则混合液一定呈碱性 |
| B、常温下,将等体积0.01mol/LHCl与pH=12的氨水混合,则混合液的pH=7 |
| C、0.1mol/L的某二元弱酸盐Na2A溶液中,c(Na+)=2c(H2A)+2c(HA?)+2c(A2-) |
| D、将5 mL 0.02mol/L的H2SO4与5 mL 0.02mol/LNaOH溶液充分混合,若混合后溶液的体积为10mL,则混合液的pH=2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定量的Fe与含1 mol HNO3的稀硝酸恰好反应,则被还原的氮原子数小于NA |
| B、1 L 1 mol/L的FeCl3溶液中含有NA个Fe3+ |
| C、常温常压下,等质量的SO2、S2含有相同的分子数 |
| D、125 g CuSO4?5H2O晶体中含有0.5NA个Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 |
| B、做银镜反应后试管壁上银镜,用稀氨水洗涤 |
| C、将0.1 mol/L的NaOH溶液与0.5 mol/L的CuSO4溶液等体积混合制得氢氧化铜浊液,用于检验醛基 |
| D、不慎将苯酚溶液沾到皮肤上,立即用NaOH溶液清洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、物质发生化学反应都伴随着能量变化 |
| B、伴有能量变化的物质变化都是化学变化 |
| C、反应热是1mol物质参加反应时的能量变化 |
| D、反应放热时△H>0,反应吸热时△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔是表示物质数量的单位 |
| B、摩尔是表示物质多少的单位 |
| C、摩尔是既能表示物质所含微粒数的数量,又能表示物质质量的具有双重意义的单位 |
| D、摩尔是巨大数目的微粒集合体,表示物质的量的国际单位 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、H2O2的电子式 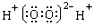 |
B、CO2的比例模型  |
C、S2-的结构示意图 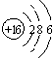 |
| D、质子数为53、中子数为72的碘原子:12553I |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、VA=0.5mol/(L?min) |
| B、VB=0.6mol/(L?min) |
| C、VC=0.35mol/(L?min) |
| D、VD=0.4mol/(L?min) |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、图中所示转化反应都不是氧化还原反应 |
| B、反应①过滤后所得沉淀为氢氧化铁 |
| C、反应②的化学方程式为NaAlO2+CO2+2H2O═Al(OH)3↓+NaHCO3 |
| D、试剂X可以是氢氧化钠溶液,也可以是盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com