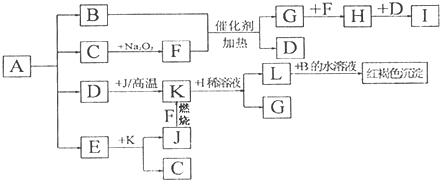
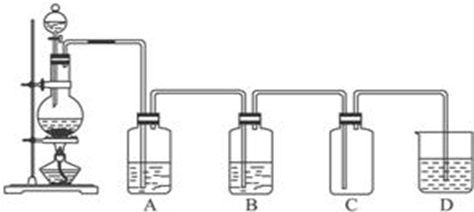
某工厂的废金属屑中主要成分为Fe和Al,此外还含有少量Al
2O
3和Fe
2O
3,该厂用上述废金属屑制取新型高效水处理剂K
2FeO
4(高铁酸钾)等产品,过程如下:
I:向废金属屑中加入过量的NaOH溶液,充分反应后过滤.该步骤中加入过量的NaOH溶液的目的是
.
Ⅱ:向I所得固体中加入过量稀H
2SO
4,充分反应后过滤,经检验所得滤液中不含Fe
3+,其原因是(用离子方程式表示)
.
Ⅲ:将Ⅱ所得滤液经进一步处理可制得Na
2FeO
4,流程如下:

(1)写出由Fe(OH)
3制取Na
2FeO
4的化学方程式
.
(2)测得滤液中c(Fe
2+)为a mol?L
-1,若要处理1m
3滤液,理论上需要消耗25%的H
2O
2溶液
kg(用含a的代数式表示).
Ⅳ:将一定量的Na
2FeO
4投入到KOH溶液,Na
2FeO
4可与KOH反应生成K
2FeO
4:
Na
2FeO
4+2KOH═K
2FeO
4+2NaOH
(1)该反应是在低温下进行的,说明此温度下K
sp(K
2FeO
4)
K
sp(Na
2FeO
4)(填“>”或“<”或“=”).
(2)K
2FeO
4在水溶液中易“水解”:4FeO
42-+10H
2O?4Fe(OH)
3+8OH
-+3O
2.在“提纯”K
2FeO
4中采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
溶液(填序号).
A.H
2O B.CH
3COONa、乙醇 C.NH
4Cl、乙醇 D.Fe(NO
3)
3、乙醇
(3)K
2FeO
4处理水时,不仅能消毒杀菌,还能除去水体中的H
2S、NH
3等,生成的Fe(OH)
3胶体还能吸附水中的悬浮杂质.根据污染物的实际情况向污水中加入适量的K
2FeO
4将污染物转化为无污染的物质,试写出K
2FeO
4处理含NH
3的污水时与NH
3反应的离子方程式
.



 阅读快车系列答案
阅读快车系列答案