
对元素周期表和元素周期律的发现有突出贡献的科学家是
A.拉瓦锡 B.阿伏加德罗 C.门捷列夫 D.道尔顿
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
 (2013?德州一模)【化学一物质结构与性质】
(2013?德州一模)【化学一物质结构与性质】查看答案和解析>>
科目:高中化学 来源: 题型:

| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | M层上有2对成对电子 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |


查看答案和解析>>
科目:高中化学 来源: 题型:
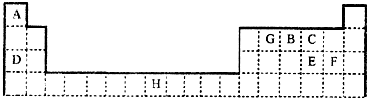
查看答案和解析>>
科目:高中化学 来源: 题型:
| X元素的基态原子中电子分布在三个不同的能级中,且每个能级中的电子总数相同 |
| Y原子的2p轨道中有3个未成对的电子 |
| Z元素的族序数是其周期数的3倍 |
| W原子的第一至第六电离能分别为:I1=578kJ/mol;I2=1817kJ/mol; I3=2745kJ/mol;I4=11575/kJ/mol;I5=14830kJ/mol;I6=18376kJ/mol |
| Q为前4周期中电负性最小的元素 |
| 元素R位于周期表的第11列 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 氟化物 | X | Y | Z |
| 熔点/K | 1266 | 1534 | 183 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com