
| A、HCl |
| B、K2SO4 |
| C、FeCl3 |
| D、NaCl |


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
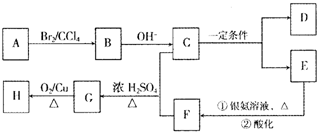
 (R、R′可以是烃基也可以是氢原子)
(R、R′可以是烃基也可以是氢原子)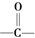 的异构体共有个
的异构体共有个查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
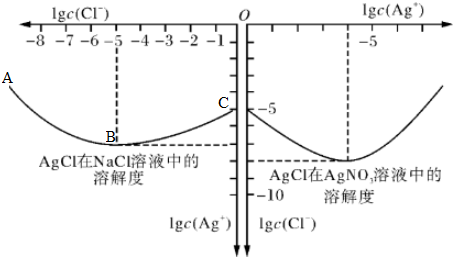
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、敞开体系,向FeCl2溶液滴加NaOH:4Fe2++8OH-+O2+2H2O=4Fe(OH)3↓ |
| B、酸性 FeSO4 溶液中加 H2O2:2Fe2++H2O2+2H+=2Fe3++2H2O |
| C、硫代硫酸钠溶液中加入稀硫酸:2H++S2O3-=S↓+SO2↑+H2O |
| D、将氧气通入酸性碘化钾溶液中:2I-+O2+4H+=I2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
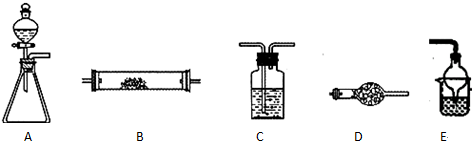
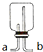 可连接在E处,则Cl2从
可连接在E处,则Cl2从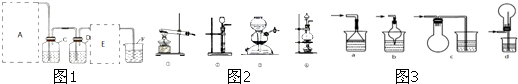
查看答案和解析>>
科目:高中化学 来源: 题型:
A、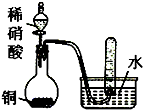 验证铜与稀硝酸的反应产物是NO |
B、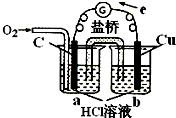 实现化学反应:2Cu+O2+4H+=2Cu2++2H2O |
C、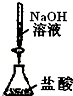 测定盐酸的浓度 |
D、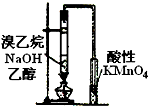 检验溴乙烷与NaOH醇溶液共热有乙烯生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com