
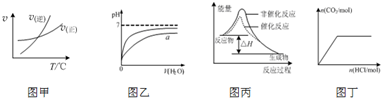
| A、由图甲表示的反应速率随温度变化的关系可知该反应的△H>0 |
| B、图乙表示pH相同的盐酸与醋酸中分别加入水后溶液pH的变化,其中曲线a对应的是醋酸 |
| C、图丙表示该反应为放热反应,且催化剂能改变反应的焓变 |
| D、图丁表示向Na2CO3溶液中逐滴滴加稀盐酸,生成CO2与所加盐酸物质的量的关系 |
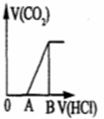 ,故D错误;
,故D错误;

 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案科目:高中化学 来源: 题型:
| A、一定产生BaSO3沉淀 |
| B、一定产生BaSO4沉淀 |
| C、产生的不全是BaSO4沉淀 |
| D、一定有SO3逸出 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 在NaCl晶体中,距Na+最近的Cl-形成正八面体 |
B、 该气态团簇分子的分子式为E4F4或F4E4 |
C、 在SiO2晶体中,1molSi原子最多可形成4molSi-O键 |
D、 单质锌采取六方最密堆积,配位数为8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、△H<0且参与反应的高氯酸钾越多,其值越小 |
| B、在该热电池中,铁为负极,发生还原反应 |
| C、正极反应式为KClO4(s)+8e-═KCl(s)+4O2-(l) |
| D、生成1mol FeO转移8mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:X>Y>Z |
| B、元素的非金属性:X>Y>Z |
| C、气态氢化物稳定性:X<Y<Z |
| D、原子序数:Z>Y>X |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将CuCl2溶液置于表面皿中加热蒸干,可制取无水CuCl2固体 |
| B、将NH4HCO3饱和溶液置于蒸发皿中加热蒸干,可制取NH4HCO3固体 |
| C、向FeCl3饱和溶液缓慢滴入过量氨水加热,可制取Fe(OH)3胶体 |
| D、用铜和浓硝酸制备NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NA个二氧化碳分子和0.5 mol甲烷的质量比为l l:4 |
| B、1molCl2体积约为22.4L |
| C、在0℃,101kPa时,11.2 L氢气中含有0.5NA个氢原子 |
| D、14 g氮气中含有7NA个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com