
 ��
�� +HBr��
+HBr��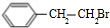 ����D-E�Ļ�ѧ����ʽ��2
����D-E�Ļ�ѧ����ʽ��2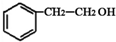 +O2$��_{��}^{����}$2
+O2$��_{��}^{����}$2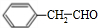 +2H2O��
+2H2O��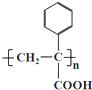
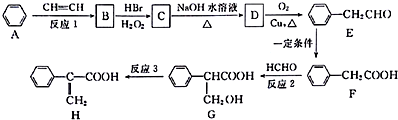
���� �ɱ�������ȩ��ת����֪��������Ȳ�����ӳɷ�Ӧ����BΪ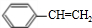 ������ϩ��HBr�����ӳɷ�Ӧ����CΪ
������ϩ��HBr�����ӳɷ�Ӧ����CΪ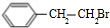 ��C����ˮ�ⷴӦ����DΪ
��C����ˮ�ⷴӦ����DΪ ��D����������Ӧ�õ�����ȩ������ȩ��һ���������ɱ����ᣬ���������ȩ�����ӳɷ�Ӧ����G��G������ȥ��Ӧ����H��
��D����������Ӧ�õ�����ȩ������ȩ��һ���������ɱ����ᣬ���������ȩ�����ӳɷ�Ӧ����G��G������ȥ��Ӧ����H��
��� �⣺�ɱ�������ȩ��ת����֪��������Ȳ�����ӳɷ�Ӧ����BΪ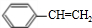 ������ϩ��HBr�����ӳɷ�Ӧ����CΪ
������ϩ��HBr�����ӳɷ�Ӧ����CΪ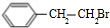 ��C����ˮ�ⷴӦ����DΪ
��C����ˮ�ⷴӦ����DΪ ��D����������Ӧ�õ�����ȩ������ȩ��һ���������ɱ����ᣬ���������ȩ�����ӳɷ�Ӧ����G��G������ȥ��Ӧ����H��
��D����������Ӧ�õ�����ȩ������ȩ��һ���������ɱ����ᣬ���������ȩ�����ӳɷ�Ӧ����G��G������ȥ��Ӧ����H��
��1����G�Ľṹ��ʽ����֪���������ŵ������ǣ��Ȼ����ǻ�����Ӧ1Ϊ�ӳɷ�Ӧ����B�Ľṹ��ʽ��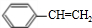 ��
��
�ʴ�Ϊ���Ȼ����ǻ���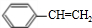 ��
��
��2����B-C�Ļ�ѧ����ʽ�ǣ�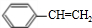 +HBr��
+HBr��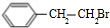 ��
��
��D-E�Ļ�ѧ����ʽ�ǣ�2 +O2$��_{��}^{����}$2
+O2$��_{��}^{����}$2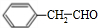 +2H2O��
+2H2O��
�ʴ�Ϊ��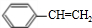 +HBr��
+HBr��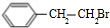 ��
��
2 +O2$��_{��}^{����}$2
+O2$��_{��}^{����}$2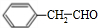 +2H2O��
+2H2O��
��3����Ӧ2�ķ�Ӧ����Ϊ�ӳɷ�Ӧ��
�ʴ�Ϊ���ӳɷ�Ӧ��
��4��a��1mol G ��������Na��Ӧ����1mol����������һ���DZ���£����������һ����22.4LH2����a����
b��G��H��д����൱�ڱ���ϩ�������ʵ�����B��G��H��ȫȼ���������������ʵ�����ȣ���b��ȷ��
c��̼̼˫���������������������ӳɷ�Ӧ��һ��������1mol�л���H�������4mol H2������Ӧ����c����
d��H���ܷ������۷�Ӧ����һ��������ͨ���Ӿ۷�Ӧ�õ� ����d����
����d����
��ѡ��b��
���� ���⿼���л�����ƶ���ϳɡ��л���Ľṹ�����ʵȣ��������չ����ŵ�������ת�����Ƕ��л���ѧ�������ۺϿ��飮


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
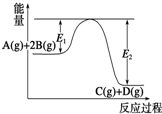
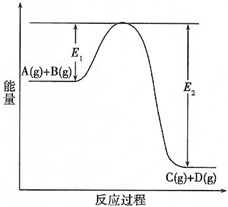
| A�� | �÷�ӦΪ���ȷ�Ӧ | |
| B�� | ����Ӧ�ﵽƽ��ʱ�������¶ȣ�A��ת�������� | |
| C�� | ѹǿ����ƽ��������Ӧ�����ƶ� | |
| D�� | �����������Ӧ��������E1��С��E2��С����Ӧ�ȼ�С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ���� | 0.01mol•L-1 ����KMnO4��Һ | 0.1mol•L-1 H2C2O4��Һ | ˮ | 1mol•L-1 MnSO4��Һ | ��Ӧ�¶� /�� | ��Ӧʱ�� |
| �� | 2mL | 2mL | 0mL | 0 | 20 | 125 |
| �� | 2mL | 1mL | 1mL | 0 | 20 | 320 |
| �� | 2mL | 2mL | 0mL | 0 | 50 | 30 |
| �� | 2mL | 2mL | 0mL | 2�� | 20 | 10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCl����ˮ | B�� | �ռ��ۻ� | C�� | H2ȼ�� | D�� | I2���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Ҫ�ɷ�ΪNaCl��NaClO��NaHCO3 | B�� | c��Cl-��=c��ClO-�� | ||
| C�� | 2c��Na+��=c��CO32-��+c��HCO3-��+c��H2CO3�� | D�� | c��Na+��=c��Cl-��+c��ClO-��+2c��CO32-��+c��HCO3-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��B��ʾ��ƽ����Ӧ����Ϊv��B��=0.0625mol•L-1•s-1 | |
| B�� | 4minʱ��A�����ʵ���Ϊ0.75mol | |
| C�� | �÷�Ӧ����ʽ�У�x=2 | |
| D�� | 4minʱ��B��ת����Ϊ25% |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com