
| X | ||||
| R |
分析 (1)根据物质的量与热量的关系以及热化学方程式的书写方法来解答;
(2)根据Q=m•c•△T计算出反应放出的热量,然后计算出生成1mol水放出的热量,就可以得到中和热
(3)由短周期元素,X元素最低负化合价的绝对值等于其原子的最外层电子数,设最外层电子数为x,则有8-x=x,x=4,则X为C元素,根据在元素周期表的相对位置可知R为S元素;
(4)设P4O10物质的量为x,P4O6物质的量为y,结合原子守恒计算得到,依据热化学方程式计算反应放出的热量.
解答 解:(1)中和热是指在稀溶液中,强酸和强碱发生中和反应生成1mol H2O时,放出57.3kJ的热量,则中和热的热化学方程式为:1/2H2SO4(aq)+NaOH(aq)=1/2Na2SO4(aq)+H2O(l)△H=-57.3 kJ/mol,
故答案为:$\frac{1}{2}$H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3 kJ/mol;
(2)50mL0.50mol/L氢氧化钠与30mL0.50mol/L硫酸溶液进行中和反应,生成水的物质的量为0.05L×0.50mol/L=0.025mol,溶液的质量为:80mL×1g/cm3=80g,温度变化的值为△T=4.0℃,则生成0.025mol水放出的热量为:Q=m•c•△T=80g×4.18J/(g•℃)×4.0℃=1337.6J,即1.3376KJ,所以实验测得的中和热△H=-$\frac{1.3376kJ}{0.025mol}$=-53.5kJ/mol;用相同浓度和体积的氨水(NH3•H2O)代替NaOH溶液进行上述实验,氨水是弱电解质,电离吸热,导致测得的中和热的数值会偏小;
故答案为:-53.5kJ/mol;偏小;
(3)由短周期元素,X元素最低负化合价的绝对值等于其原子的最外层电子数,设最外层电子数为x,则有8-x=x,x=4,则X为C元素,根据在元素周期表的相对位置可知R为S元素;由X和R形成的液态化合物为CS2,根据燃烧热可写出反应的热化学方程式为
CS2(l)+3O2(g)=CO2(g)+2SO2(g)△H=-1075kJ/mol;CS2是直线型分子,其结构式为S=C=S;
故答案为:CS2(l)+3O2(g)=CO2(g)+2SO2(g)△H=-1075kJ/mol;S=C=S;
(4)在某密闭容器中加入62g白磷和50.4L氧气(标准状况),白磷中磷原子物质的量=$\frac{62g}{31g/mol}$=2mol原子,氧气物质的量=$\frac{50.4L}{22.4L/mol}$=2.25mol,含有4.5mol氧原子;依据原子守恒列式计算:设P4O10物质的量为x,P4O6物质的量为y
$\left\{\begin{array}{l}{4x+4y=2mol}\\{5x+3y=2.25mol}\end{array}\right.$
计算出x=0.375mol,y=0.125mol
最后生成0.375molP4O10,0.125molP4O6mol,故物质的量之比为3:1;
P4(白磷,s)+3O2(g)═P4O6(s)△H=-1 638kJ•mol-1;
P4(白磷,s)+5O2(g)═P4O10(s)△H1=-2 983.2kJ•mol-1;
放出的热量=0.375mol×(-2983.2KJ/mol)+0.125 mol×(-1638KJ/mol)=1323.45kJ;
故答案为:3:1;1323.45 kJ.
点评 本题考查了物质结构分析,热化学方程式书写和盖斯定律计算应用,原子守恒和化学方程式的计算方法应用,掌握基础是关键,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
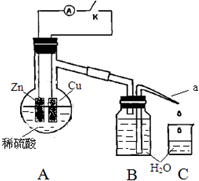 某同学分析Zn与稀H2SO4的反应.
某同学分析Zn与稀H2SO4的反应.| 1分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
| 1分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三种 | B. | 四种 | C. | 五种 | D. | 六种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
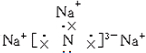 ,该化合物由离子键形成.
,该化合物由离子键形成.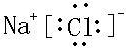 ,
, .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Na>Mg>O | |
| B. | 13C和14C属于同位素 | |
| C. | 0族元素是同周期中非金属性最强的元素 | |
| D. | N和P属于第ⅤA族元素,HNO3酸性比H3PO4的强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
 ;G、H 氢化物的稳定性递减的顺序是HCl>HBr.
;G、H 氢化物的稳定性递减的顺序是HCl>HBr. ;.
;. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1,3-丁二烯(CH2=CH-CH=CH2)与等物质的量的Br2发生加成反应 | |
| B. | 2-氯丁烷( )与NaOH乙醇溶液共热发生消去HCl分子的反应 )与NaOH乙醇溶液共热发生消去HCl分子的反应 | |
| C. | 甲苯在一定条件下与足量硝酸发生硝化反应 | |
| D. | 乙醇与HBr发生的取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
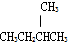 D、
D、 和
和 E、CH3CH2CH2CH3和
E、CH3CH2CH2CH3和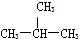
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com