
【题目】一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示,下列说法正确的是( )
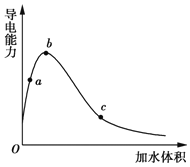
A. a、b、c三点溶液的pH:c<a<b
B. 用湿润的pH试纸测量a处溶液的pH,测量结果偏小
C. a、b、c三点CH3COOH的电离程度:c<a<b
D. a、b、c三点溶液用1 mol·L-1NaOH溶液中和,消耗NaOH溶液体积:c<a<b
【答案】B
【解析】
A.导电能力越强,离子浓度越大,氢离子浓度越大,pH越小;
B.a处溶液稀释时,溶液酸性增强;
C.随水的增多,醋酸的电离程度增大;
D.a、b、c三点溶液浓度不同,但溶质的物质的量相同。
A.导电能力越强,离子浓度越大,氢离子浓度越大,pH越小,则a、b、c三点溶液的pH为b<a<c,A错误;
B.用湿润的pH试纸测量酸性的pH,a处溶液稀释,导电能力增大,溶液酸性增强,pH减小,所以测量结果偏小,B正确;
C.随水的增多,醋酸的电离程度增大,所以a、b、c三点醋酸的电离程度:a<b<c,C错误;
D.a、b、c三点溶液浓度不同,但溶质的物质的量相同,所以a、b、c三点溶液用1mol/L氢氧化钠溶液中和,消耗氢氧化钠溶液体积:a=b=c,D错误;
答案选B。


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ.用化学用语回答下列问题:
(1)写出二氧化碳分子的电子式:_______;
(2)写出氮气分子的结构式______。
Ⅱ.下列物质:①N2 ②CO2 ③NH3 ④Na2O ⑤Na2O2 ⑥NaOH ⑦CaBr2 ⑧H2O2 ⑨NH4Cl ⑩C2H6,含有极性键和非极性键的是_____;(填序号)
Ⅲ.下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4熔融;④硫酸溶于水;⑤蔗糖溶于水;⑥HI分解;⑦ 碘升华;⑧溴蒸气被木炭吸附。
(1)未破坏化学键的是____;(填序号)
(2)仅离子键被破坏的是___。(填序号)
Ⅳ.下列物质:①1H、2H、3H;②H2O、D2O、T2O;③O2、O3;④14N、14C
(1)互为同位素的是:_____;(填序号)
(2)互为同素异形体的是:____;(填序号)
(3)氢的三种原子1H、2H、3H与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有_____种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应![]() 达到平衡,正反应速率随时间变化的示意图如下所示。
达到平衡,正反应速率随时间变化的示意图如下所示。

A. 反应在c 点达到平衡状态
B. 反应物浓度:![]() 点小于
点小于![]() 点
点
C. 反应物的总能量低于生成物的总能量
D. ![]() 时,SO2的转化率:
时,SO2的转化率:![]() 段小于
段小于![]() 段
段
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过下列两步实验测定草酸晶体(H2C2O4·xH2O)中结晶水x的值:
①称取2.52 g草酸晶体,配制成100 .00 mL溶液。
②取25.00 mL所配溶液置于锥形瓶中,加入适量稀硫酸后,用浓度为0.100 mol·L-1 KMnO4溶液进行滴定。其反应原理是:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O
请回答下列问题:
(1)实验②中,KMnO4应装在______滴定管中(填“酸式”、“碱式”)。
(2)如图表示50mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积______。
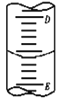
A.是amL B.是(50-a)mL
C.一定大于amL D.一定大于(50-a)mL
(3)判断达到滴定终点的现象是_____________________________;
若滴定终点时,共用去KMnO4溶液20.00 mL,则x =__________。
(4)若在滴入KMnO4溶液之前滴定管的尖嘴部分有气泡,滴定结束后气泡消失,则会使测定结果______(偏高、偏低或无影响)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向NaOH和Na2CO3混合溶液中滴加0.1mol/L盐酸,CO2的生成量与加入盐酸的体积(V)的关系如图所示,下列判断正确的是( )
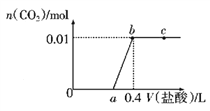
A. a点时溶液中存在c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)
B. 0~a段溶液中水电离出的OH-浓度先增大后减小
C. a=0.2
D. ab段发生反应的离子方程式为CO32-+2H+=H2O+CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为周期表中短周期的一部分。已知a原子的最外层上的电子数目是次外层电子数目的一半,下列说法中不正确的是( )

A. 元素a的最高价氧化物的水化物的酸性比b弱
B. 元素a的原子半径比d的大
C. 元素a的单质在空气中燃烧会导致“温室效应”
D. 元素a单质是一种良好的半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z、R 原子序数依次增大。由W、X、Y、R组成的一种化合物a在加热时完全分解为三种产物,其中一种产物b是能使品红溶液褪色的气体,另一种产物c是能使湿润的红色石蕊试纸变蓝的气体。金属单质Z在空气中燃烧生成的化合物可与水发生反应生成气体。下列说法正确的是
A. 简单离子的半径: X < Z < R
B. X的简单氢化物比Y的稳定
C. a、b、c中均含有极性共价健,且 a属于电解质,b和c都属于非电解质
D. W、X、Y、R四种元素形成的化合物一定会促进水的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向20mLxmol/LCH3COOH溶液中逐滴加入等物质的量浓度的NaOH溶液,混合液的pH随NaOH溶液的体积(V)的变化关系如下图所示(忽略温度变化)。下列说法中不正确的是
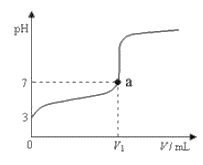
A. 上述CH3COOH溶液中:c(H+)=1×10-3mol/L
B. 图中V1<20mL
C. a点对应的溶液中,c(CH3COO-)=c(Na+)
D. 当加入NaOH溶液的体积为20mL时,溶液中:c(CH3COOH)+c(H+)>c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com