
| A. | HCN为V形分子 | |
| B. | NO3-的空间构型为三角锥形 | |
| C. | SF6中有6对完全相同的成键电子对 | |
| D. | SO42-和SO32-的中心原子均为sp3杂化 |
分析 A.HCN的结构为H-C≡N,C原子没有孤电子对;
B.根据价层电子对个数=σ键个数+孤电子对个数计算判断;
C.根据SF6中S原子的成键电子对数和孤电子对数判断;
D.先判断价层电子对数再判断杂化类型.
解答 解:A.HCN的结构为H-C≡N,C原子没有孤电子对,为直线形,故A错误;
B.NO3-中N原子的价层电子对数=3+$\frac{1}{2}$(5+1-2×3)=3,为sp2杂化,没有孤电子对,所以平面三角形,故B错误;
C.SF6中S的价层电子对数=6+$\frac{1}{2}$(6+6×1)=6,没有孤电子对,所以SF6中有6对完全相同的成键电子对,故C正确;
D.SO42-中S的价层电子对数=4+$\frac{1}{2}$(6+2-4×2)=4,为sp3杂化,SO32-的价层电子对数=3+$\frac{1}{2}$(6+2-4×2)=3,为sp2杂化,故D错误.
故选C.
点评 本题考查了微粒空间构型的判断,利用价层电子对互斥理论分析解答即可,难点是孤电子对的计算方法,题目难度不大.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
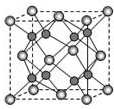
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
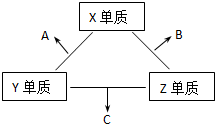 X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化:
X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化: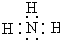 ,C分子的结构呈三角锥形.
,C分子的结构呈三角锥形.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制的氯水在光照下颜色变浅 | |
| B. | NO2和N2O4平衡混合气缩小体积加压后颜色变深 | |
| C. | 硫酸工业上SO2氧化成SO3,宜采用空气过量 | |
| D. | 煅烧硫铁矿利于SO2的生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下浓硫酸能使铝发生钝化,可在常温下用铝制容器贮藏贮运浓硫酸 | |
| B. | 氯气具有强氧化性,因此可用于漂白有色布料 | |
| C. | NH3能与Cl2生成NH4Cl,可用浓氨水检验输送氯气的管道是否有泄漏 | |
| D. | 氢氟酸能与二氧化硅反应,因此可用于刻蚀玻璃 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 混合液 | A | B | C | D | E | F |
| 4mol•L-1H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | ①③④ | B. | ①④ | C. | ②③⑤ | D. | 除② |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com