
【题目】若已知反应 NaNO2+HF═HNO2+NaF,7.2×10﹣4、4.6×10﹣4分别是上式所涉及的两种酸的电离常数.由此可判断下列叙述中不正确的是( )
A.K(HF)=c(F﹣)c(H+)/c(HF )
B.K(HNO2)=7.2×10﹣4
C.酸性强弱为 HF>HNO2
D.K(HNO2)<K(HF)
【答案】B
【解析】解:A.HF为弱酸,电离平衡常数= ![]() ,故A正确;
,故A正确;
B.若已知反应 NaNO2+HF═HNO2+NaF,则HF酸性强于HNO2,K(HNO2)=4.6×10﹣4,故B错误;
C.若已知反应 NaNO2+HF═HNO2+NaF,则HF酸性强于HNO2,故C正确;
D.HF酸性强于HNO2,电离平衡常数越大酸性越强,K(HNO2)<K(HF),故D正确;
故选B.
【考点精析】根据题目的已知条件,利用弱电解质在水溶液中的电离平衡的相关知识可以得到问题的答案,需要掌握当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理.


科目:高中化学 来源: 题型:
【题目】丙烷在燃烧时能放出大量的热,它也是液化石油气的主要成分,作为能源应用于人们的日常生产和生活。已知:
①2C3H8(g) + 7O2 (g)= 6CO(g) + 8H2O(l) △H1=-2741.8 kJ/mol
②2CO(g)+O2(g)= 2CO2(g) △H2 =-566 kJ/mol
(1) 反应C3H8(g) + 5O2(g)= 3CO2(g) + 4H2O (1) 的△H=_______。
(2) 现有lmol C3H8 在不足量的氧气里燃烧,生成1mol CO 和2mol CO2 以及气态水,将所有的产物通入一个固定体积为1L 的密闭容器中,在一定条件下发生如下可逆反应:CO(g)+ H2O (g) ![]() CO2(g)+H2(g) △H= +4 1.2 kJ/mol
CO2(g)+H2(g) △H= +4 1.2 kJ/mol
①下列事实能说明该反应达到平衡的是______
a.体系中的压强不发生变化
b.v正(H2) = v逆(CO)
c.混合气体的平均相对分子质量不发生变化
d.CO2的浓度不再发生变化
②5min 后体系达到平衡,经测定,H2 为0.8mol,则平衡常数K=_______。
③其他条件不变,向平衡体系中充入少量CO 则平衡常数_____ (填增大、减小或不变)。
(3) 依据(1)中的反应可以设计一种新型燃料电池,一极通入空气,另一极通入丙烷气体;燃料电池内部是熔融的掺杂着氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在其内部可以传导O2-。在电池内部O2-由______极移向______ 极(填“正”或“负”);电池的负极电极反应式为____________。
(4) 用上述燃料电池和惰性电极电解足量Mg(NO3)2 和NaCl 的混合溶液。电解开始后阴极的现象为____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知氯化银在水中的溶解平衡为: AgCl(s)Ag+(aq)+Cl﹣(aq),
25℃,其Ksp为:Ksp=[Ag+][Cl﹣]=1.8×10﹣10 mol2L﹣2 . 现把氯化银(足量)分别放人:
①100mL蒸馏水中;
②100mL 0.1molL﹣1的盐酸溶液中;
③1000mL 0.1molL﹣l的氯化铝溶液中;
④100mL0.1molL﹣1的氯化镁溶液中.
充分搅拌后,相同温度下,银离子浓度由大到小的顺序是(用序号回答) . 在0.1molL﹣l氯化铝溶液中,银离子的物质的量浓度最大可达到 .
查看答案和解析>>
科目:高中化学 来源: 题型:
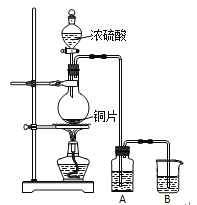
【题目】I.实验室用下图装置制取并研究SO2的性质。
完成下列填空:
(1)圆底烧瓶中反应的化学方程式为_____________________________________。
(2)若A中盛放品红溶液,可以验证的SO2性质是______________。若要验证SO2的还原性,A中应盛放_________溶液。B中应盛放_________溶液。
II.为测定反应后的溶液中残留的硫酸浓度,实验小组进行如下探究。
(3)甲组:取1 mL反应液加水稀释至100 mL,再取10 mL稀释液与足量锌粒用下图装置进行测定。在读取反应前后量气管中液面读数时应先调节水准管与量气管中液面等高,这样操作的目的是________。
实验测得反应生成的氢气体积为22.4 mL(已换算到标准状况),计算原反应液中残留的硫酸浓度为______mol/L。

(4)乙组:欲通过加入足量的BaCl2溶液,测定生成的BaSO4沉淀质量来达到实验目的。该设计思路不可行,理由是_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生产生活和科学研究中具有重要的作用。下列说法正确的是( )
①耐高温的碳化硅陶瓷是新型无机非金属材料
②现代建筑物大量使用的沙子和水泥都是硅酸盐材料
③单质硅可以用来制造太阳能电池
④水晶项链和陶瓷都是硅酸盐材料
A.①②B.②③C.②④D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知气态烃A中碳的质量分数为92.3%,C与D互为同分异构体,F含有两个与乙醇相同的官能团,有关物质的转化关系如图:
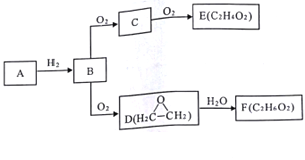
请回答:
(1)写出B的电子式___________________。
(2)C→E的反应类型___________________。
(3)D→F的化学方程式___________________。
(4)下列说法正确的是___________________。
A. 可用燃烧法鉴别A和B
B. C在一定条件下可与氢气发生还原反应
C. E和F在浓硫酸作用下加热反应,产物只有一种
D. 与D的最简式相同,相对分子质量为88的物质可能是E的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向稀硫酸溶液中逐渐加入氨水,当溶液中c(NH4+)=2c(SO42﹣)时,溶液的pH( )
A. 大于7 B. 等于7 C. 小于7 D. 无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意填空:
(1)碳酸钠溶液中各离子按照浓度从大到小的顺序依次为: .
(2)下表是几种常见弱酸的电离平衡常数(25℃)
酸 | H2CO3 | CH3COOH | HClO |
K | K1=4.4×10﹣7;K 2=4.7×10﹣11 | K=1.76×10﹣5 | K=2.95×10﹣8 |
根据分析表格中数据可知,H2CO3、CH3COOH、HClO 三种酸的酸性从强到弱依次是;25℃时,等浓度的Na2CO3、NaAc 和NaClO三种溶液的pH从小到大依次是 .
(3)常温下,将0.02molL﹣1 的 Ba(OH)2溶液100mL和0.02molL﹣1的NaHSO4溶液100mL混合,若忽略溶液体积变化,则混合后的溶液的 pH 为 .
(4)25℃时,Ksp[Mg(OH)2]=5.61×10﹣12 , Ksp[MgF2]=7.42×10﹣11 . 该温度下饱和Mg(OH)2溶液与饱和 MgF2溶液相比,(填化学式)溶液中的 c(Mg2+)大.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于“观察DNA和RNA在细胞中的分布”的实验,下列说法中正确的是( )
A. 染色时先用甲基绿染液,再用吡罗红染液
B. 用质量分数为8%的盐酸的目的之一是使DNA与蛋白质分离,并使DNA水解
C. 酒精灯烘干载玻片,可将细胞固定在载玻片上
D. 用高倍显微镜可以比较清楚地看到呈现绿色的染色体和呈现红的RNA分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com