
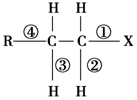
| A. | 发生水解反应时,被破坏的键是④ | |
| B. | 发生消去反应时,被破坏的键是①和② | |
| C. | 发生水解反应时,被破坏的键是①和④ | |
| D. | 发生消去反应时,被破坏的键是①和③ |
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 A、B、C、D为短周期主族元素,25℃时,其最高价氧化物的水化物溶液(浓度均为0.1mol•L-1)的pH和原子序数的关系如图所示.下列有关说法正确的是( )
A、B、C、D为短周期主族元素,25℃时,其最高价氧化物的水化物溶液(浓度均为0.1mol•L-1)的pH和原子序数的关系如图所示.下列有关说法正确的是( )| A. | 简单离子半径:D离子>C离子>A离子>B离子 | |
| B. | D元素氧化物的水化物一定是强酸 | |
| C. | B、C的简单离子都能破坏水的电离平衡 | |
| D. | 氢化物还原性:C>D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | IBr 与 AgNO3 溶液反应会生成浅黄色沉淀 | |
| B. | IBr 与水反应属于氧化还原反应,IBr 既作氧化剂又作还原剂 | |
| C. | IBr 属于共价化合物 | |
| D. | 反应 IBr+2Na=NaBr+NaI 中,每反应 2mol Na,电子转移数目为 2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 普通肥皂的主要成分是高级脂肪酸钠盐 | |
| B. | 利用氢化反应将液态植物油转变为固态反式脂肪酸的过程发生的是还原反应 | |
| C. | “皮革奶粉”含有大量有毒物质,不能食用 | |
| D. | 沾有血迹的衣物要用热水和加酶洗衣粉浸泡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
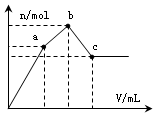 浓度为 0.1mol•L-1硫酸铝铵[NH4Al(SO4)2]溶液100mL中,逐滴滴入0.1mol•L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )
浓度为 0.1mol•L-1硫酸铝铵[NH4Al(SO4)2]溶液100mL中,逐滴滴入0.1mol•L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.则下列说法中正确的是( )| A. | a点对应的沉淀,其物质的量为0.01mol | |
| B. | b点发生反应的离子方程式是:Al3++2SO42-+2Ba2++3OH-═Al(OH)3↓+2BaSO4↓ | |
| C. | 沉淀质量最大值为4.66g | |
| D. | c点加入Ba(OH)2溶液的体积为250 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 除去苯中的甲苯,可使用酸性 KMnO4和 NaOH,然后分液 | |
| B. | 除去乙醇中混有的少量乙酸,加 NaOH 溶液,然后分液 | |
| C. | 检验溴乙烷中溴元素,直接加入硝酸银溶液生成浅黄色沉淀 | |
| D. | 实验室制备乙烯时,产生的气体直接通入溴水,溴水褪色,证明有乙烯生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com