


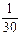 mol/L (2分)
mol/L (2分)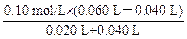 =
=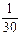 mol/L (2分)
mol/L (2分)

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源:不详 题型:填空题
| 实验编号 | HA物质的量浓度(mol/L) | NaOH物质的量浓度(mol/L) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
 (填﹥、﹤或=),该混合溶液中离子浓度由大到小的顺序是_____ ___。
(填﹥、﹤或=),该混合溶液中离子浓度由大到小的顺序是_____ ___。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.a = 20.00 |
| B.滴定过程中,可能存在:c(Cl-)>c(H+)>c(Na+)>c(OH-) |
| C.若用酚酞作指示剂,当滴定到溶液明显由无色变为红色时停止滴定 |
| D.若将盐酸换成同浓度的醋酸,则滴定到pH=7时,a>20.00 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在Na2CO3溶液中加入与其溶质等物质的量的冰醋酸,溶液中存在: c(Na+) = c(CH3COOH) + c(CH3COO-)+ c(CO  )+c(HCO )+c(HCO ) + c(H2CO3) ) + c(H2CO3) |
| B.NaHCO3溶液中存在:c(H+)+c(H2CO3)=c(OH-) |
| C.10 mL 1.0 mol·L-1CH3COOH溶液中加入0.01 mol的NaOH后,溶液中离子浓度的大小关系为:c(Na+)=c(CH3COO-)>c(OH-)=c(H+) |
| D.相同条件下,中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量前者大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.将醋酸逐滴加入醋酸钠溶液中至溶液呈酸性,则该混合液中: C(Na+)>C(CH3COO-)>C(H+)>C(OH-) |
| B.将0.1mol/LCH3COOH溶液加水稀释,在此过程中,醋酸的电离程度、溶液的PH都逐渐增大 |
| C.在碳酸氢钠溶液中加入与其等物质的量的烧碱,溶液中的阴离子只有CO3-和OH- |
| D.常温下,将PH==12的烧碱溶液与PH==2的醋酸溶液等体积混合,所得混合溶液的PH>7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.两种溶液中,由水电离出的氢离子浓度均为1×10-11 mol/L |
| B.分别加水稀释100倍后,两种溶液的pH仍相同 |
| C.醋酸中的c(CH3COO-)和硫酸中的c(SO)相等 |
| D.分别加入足量锌片,两种溶液生成H2的体积相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.相等 | B.x>y | C.x=10-2y | D.x=102y |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com