
 和
和 ; ②
; ② 和
和 ;
;| 类别 | 同系物 | 同素异形体 | 同分异构体 |
| 组号 |
 和
和 都是烷烃,根据烷烃的命名原则进行解答.
都是烷烃,根据烷烃的命名原则进行解答.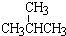 和
和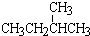 结构相似,分子组成相差1个“CH2”原子团,互为同系物;
结构相似,分子组成相差1个“CH2”原子团,互为同系物; 和
和 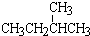 分子式相同,但结构不同,互为同分异构体;
分子式相同,但结构不同,互为同分异构体; 根据烷烃的命名原则,该有机物名称为:2,2-二甲基丙烷或新戊烷;
根据烷烃的命名原则,该有机物名称为:2,2-二甲基丙烷或新戊烷; 为异戊烷或2-甲基丁烷,
为异戊烷或2-甲基丁烷,| 同系物 | 同素异形体 | 同分异构体 | |
| 组号 | ①③ | ④⑧ | ②⑦ |


科目:高中化学 来源: 题型:
 电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.模拟处理装置如图所示,下列说法错误的是( )
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.模拟处理装置如图所示,下列说法错误的是( )| A、X电极是负极,电极反应式为:CH4-8e-+4CO32-═5CO2+2H2O |
| B、铁是阳极,失去电子生成Fe2+ |
| C、工作时熔融盐中的碳酸根移向Y电极 |
| D、污水中存在反应:4Fe2++10H2O+O2═4Fe(OH)3↓+8H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
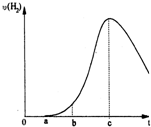 把在空气中久置的铝片5.0g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图坐标曲线来表示,回答下列问题:
把在空气中久置的铝片5.0g投入盛有500mL 0.5mol?L-1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率与反应时间可用如图坐标曲线来表示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
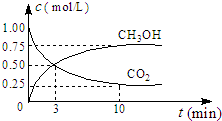 联合国气候变化大会于2009年12月7-18日在哥本哈根召开.中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.
联合国气候变化大会于2009年12月7-18日在哥本哈根召开.中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~45%.
| ||
| ||
| ||
| 太阳光 |
| 高温 |
| n(CH3OH) |
| (CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
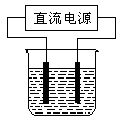 以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一.
以电解食盐水为基础制取氯气等产品的工业称为“氯碱工业”,它是目前化学工业的重要支柱之一.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+ H+ NO3- Fe2+ |
| B、Ca2+ NO3- HCO3- OH- |
| C、K+ H+ Cl- SO42- |
| D、Fe3+ Cl- H+ CO32- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com