
传统的自来水消毒常采用漂白粉等强氧化剂,但其产生的有机氯对人体有一定的危害。一种新型的消毒剂——高铁酸盐(如Na2FeO4或K2FeO4)能有效地杀灭水中的细菌和病毒,同时其产物在水中经过变化后能除去水中的微细悬浮物。在以上变化过程中不可能涉及的变化有( )
A . 电离 B. 水解 C. 置换反应 D. 氧化还原反应
科目:高中化学 来源: 题型:
下列说法中正确的是
A.1 L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol/L
B.从1 L 2 mol/L的H2SO4溶液中取出0.5 L,该溶液的浓度为1 mol/L
C.配制500 mL 0.5 mol/L的CuSO4溶液,需62.5 g胆矾
D.中和100 mL 1 mol/L的H2SO4溶液,需NaOH 4 g
查看答案和解析>>
科目:高中化学 来源: 题型:
工业上以黄铁矿为原料生产硫酸,其中重要的一步是催化氧化(生产中保持恒温恒容条件):2SO2(g)+O2(g)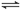 2SO3(g) △H=-196.6 kJ·mol-1
2SO3(g) △H=-196.6 kJ·mol-1
(1)生产中为提高反应速率和SO2的转化率,下列措施可行是 。
A.向装置中充入O2 B.升高温度
C.向装置中充入N2 D.向装置中充入过量的SO2
(2)恒温恒压,通入3mol SO2 和2mol O2 及固体催化剂,平衡时容器内气体体积为起始时的90%。保持同一反应温度,在相同容器中,将起始物质的量改为 5mol SO2(g)、3.5 mol O2(g)、1mol SO3(g),下列说法正确的是
 A.第一次平衡时反应放出的热量为294.9kJ
A.第一次平衡时反应放出的热量为294.9kJ
B.两次平衡SO2的转化率相等
C.两次平衡时的O2体积分数相等
D.第二次平衡时SO3的体积分数等于2/9
(3)500 ℃时将10 mol SO2和5.0 mol O2置于体积为1L的恒容密闭容器中,SO2转化为SO3的平衡转化率为0.95。则500℃时的平衡常数K= 。
(4)550 ℃,A、B表示不同压强下的平衡转化率(如图),
通常工业生产中采用常压的原因是 ,
并比较不同压强下的平衡常数:K(0.10 MPa) K(1.0 MPa)。
查看答案和解析>>
科目:高中化学 来源: 题型:
肼(N2H4)—空气燃料电池是一种环保碱性燃料电池,其电解质溶液是20%—30%的KOH溶液。电池总反应为:N2H4+O2=N2↑+2H2O。下列关于该燃料电池工作时的说法正确的是( )
A.电池工作时,负极附近溶液的碱性增强
B.正极的电极反应式是:O2+4H++4e-=2H2O
C.负极的电极反应式是:N2H4+4OH――4e-=4H2O+N2↑
D.溶液中阴离子向正极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关化学用语表示正确的是( )
 A.CaH2的电子式:[H:]-Ca2+[:H]- B.Cl-的结构示意图:
A.CaH2的电子式:[H:]-Ca2+[:H]- B.Cl-的结构示意图: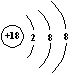
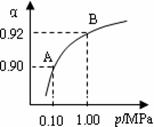
C.质子数为92、中子数为146的U原子: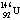 D.CH2F2的电子式:
D.CH2F2的电子式:
查看答案和解析>>
科目:高中化学 来源: 题型:
关于Na2CO3和NaHCO3性质的说法,正确的是( )
A.热稳定性:NaHCO3 > Na2CO3
B.与澄清石灰水反应:Na2CO3、NaHCO3溶液中均有沉淀生成
C.相同温度时,在水中的溶解性:NaHCO3 > Na2CO3
D.等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同
查看答案和解析>>
科目:高中化学 来源: 题型:
下列除去杂质的方法正确的是( )
| 物质 | 杂质 | 试剂 | 主要操作 | |
| A | NaHCO3固体 | Na2CO3固体 | / | 加热 |
| B | SiO2 | Fe2O3 | 盐酸 | 过滤 |
| C | KBr溶液 | Br2 | KOH溶液 | 分液 |
| D | Cl2 | HCl | 饱和碳酸钠溶液 | 洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
熔融状态下,Na的单质和FeCl2能组成可充电电池(装置示意图如下),反应原理为:
2Na+ FeCl2 Fe+ 2NaCl
Fe+ 2NaCl
放电时,电池的正极反应式为 ;充电时, (写物质名称)电极接电源的负极;该电池的电解质为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
绿色化学中,最理想的“原子经济”是原子利用率为100%。下列反应类型能体现“原子经济性”原则的是 ( )
①取代反应 ②加成反应 ③酯化反应 ④水解反应 ⑤加聚反应
A. ②⑤ B. ①② C. ③④ D. ②④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com