
| X(g)+Y(g)?CH3OH(g)+D(g) (未配平) | A(g)+B(g)?2C(g) |
分析 (1)水分解得到的可燃气体为氢气,则X为氢气;空气中能被NaOH吸收的气体为CO2,则Y为CO2、Z为Na2CO3;CO2与氢气反应生成甲醇;
(2)①n=2.5时,I中气体初始物质的量为:2.5 mol+6.5 mol+2 mol+2 mol=13 mol,Ⅱ中气体的物质的量始终为12 mol,如要是隔板停留在中间,左侧反应应向正反应方向移动,以使气体体积得到12 mol;
令达平衡时E的消耗量为2amol,求出平衡时各组分的物质的量,利用反应混和物总的物质的量为12mol列出等式,再利用可逆反应反应物不能完全反应列不等式,联立求解;
②这两种情况是在两个不同温度下达到化学平衡的,平衡状态不同,所以A的物质的量也不同.
解答 解:(1)水分解得到的可燃气体为H2;故X为氢气;空气中能被NaOH吸收的气体为CO2,即Y为CO2、Z为Na2CO3;CO2与氢气反应生成甲醇,CO2+3H2=CH3OH+H2O;
故答案为Na2CO3:;CO2+3H2=CH3OH+H2O;
(2)①n=2.5时,I中气体初始物质的量为:2.5 mol+6.5 mol+2 mol+2 mol=13 mol,Ⅱ中气体的物质的量恒为12 mol.如要是隔板停留在中间,左侧反应应向正反应方向移动,以使气体体积得到12 mol;
要使反应向正方向进行,左侧气体的初始物质的量应大于12 mol,故:n mol+10.5 mol>12 mol,即n>1.5,同时还要求,当CO2或H2完全转化为产物时,气体总物质的量应小于12 mol,若CO2完全转化,生成CH3OH和H2O物质的量均为6.5 mol,已经大于12 mol,故应为氢气完全转化时,气体总物质的量小于12 mol,故有:6.5 mol-n mol/3+4 mol+2n mol/3<12 mol,n<4.5.n的取值范围为1.5<n<4.5;
故答案为:正反应;1.5<n<4.5;
②当n取值3.0和4.0时,反应达平衡时总物质的量均为12 mol时,反应的转化率不同,反应温度不同,故平衡时A的物质的量不同;
故答案为:不相等;温度不同.
点评 本题考查化学平衡的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,难度中等,关键在于确定左侧反应到达平衡时反应混合物总的物质的量和影响化学平衡的因素.


 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:解答题
| 键 | H-H | N-H | N-N | N=N | N≡N |
| 键能/kJ•mol-1 | 436 | 391 | 159 | 418 | 945 |
| 分子式 | 结构简式 | 熔点 | 沸点 | 水溶性 | |
| 乙醇 | C2H6O | C2H5OH | -114.3℃ | 78.4°C | 互溶 |
| 二甲醚 | C2H6O | CH3OCH3 | -138.5℃ | -24.9℃ | 微溶 |
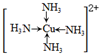 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
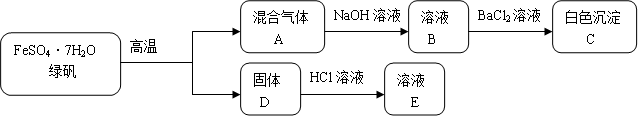
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
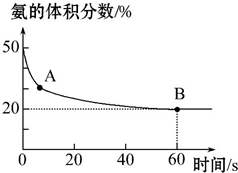 氨气是一种重要的化工原料,在工农业中都有广泛的应用.
氨气是一种重要的化工原料,在工农业中都有广泛的应用.| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡气体总浓度 (10-3mol•L-1) | 2.4 | 3.4 | 4.8 | 6.8 | 9.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g),随温度升高,混合气体的颜色变深.回答下列问题:
在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)?2NO2(g),随温度升高,混合气体的颜色变深.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
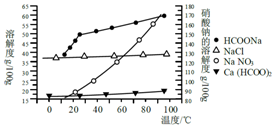 甲酸钙广泛用于食品、化工、石油等工业生产上,300~400℃左右分解.
甲酸钙广泛用于食品、化工、石油等工业生产上,300~400℃左右分解.| 金属 离子 | 开始沉淀 的pH | 沉淀完全 的pH |
| Fe3+ | 1.1 | 3.2 |
| Al3+ | 3.0 | 5.0 |
| Fe2+ | 5.8 | 8.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com