
����Ŀ�������£��������ܵ���ʵ��ܶȻ����±���
���� | Ag2CrO4 | AgCl | AgBr |
Ksp | 1.0��10-12 | 1.8��10-10 | 7.7��10-13 |
����˵����ȷ����
A. ��AgCl��Һ��ͨ������HCl���壬��Һ��c(Ag+)����
B. Ũ�Ⱦ�Ϊ1��10-6 molL��1��AgNO3��HBr��Һ�������Ϻ������AgBr����
C. �����£���0.01 molL��1 AgNO3��Һ�ζ�20mL0.01molL��1KCl��0.01molL��1K2CrO4�Ļ����Һ��CrO42-�ȳ���
D. ������,Ag2CrO4��s��+2Cl-��aq��![]() 2AgCl��s��+CrO42-��aq����ƽ�ⳣ��K=3.1��107
2AgCl��s��+CrO42-��aq����ƽ�ⳣ��K=3.1��107
���𰸡�D
��������A���ڱ���AgCl��Һ�д����ܽ�ƽ�⣺AgCl��s��![]() Ag+��aq��+Cl-��aq����ͨ��HCl��������ˮ�����Cl-��Cl-Ũ�������ܽ�ƽ�������ƶ�����Һ��c��Ag+����С��A�����B��Ũ�Ⱦ�Ϊ1
Ag+��aq��+Cl-��aq����ͨ��HCl��������ˮ�����Cl-��Cl-Ũ�������ܽ�ƽ�������ƶ�����Һ��c��Ag+����С��A�����B��Ũ�Ⱦ�Ϊ1![]() 10-6mol/L��AgNO3��HBr��Һ�������Ϻ�c��Ag+����c��Br-����Ϊ5
10-6mol/L��AgNO3��HBr��Һ�������Ϻ�c��Ag+����c��Br-����Ϊ5![]() 10-7mol/L����ʱQc=c��Ag+����c��Br-��=5
10-7mol/L����ʱQc=c��Ag+����c��Br-��=5![]() 10-7
10-7![]() 5
5![]() 10-7=2.5
10-7=2.5![]() 10-13
10-13![]() 7.7
7.7![]() 10-13����������AgBr������B�����C��Cl-��ʼ��������Ag+Ũ��Ϊc��Ag+��=Ksp��AgCl��
10-13����������AgBr������B�����C��Cl-��ʼ��������Ag+Ũ��Ϊc��Ag+��=Ksp��AgCl��![]() c��Cl-��=1.8
c��Cl-��=1.8![]() 10-10
10-10![]() 0.01=1.8
0.01=1.8![]() 10-8��mol/L����CrO42-��ʼ��������Ag+Ũ��Ϊc��Ag+��=
10-8��mol/L����CrO42-��ʼ��������Ag+Ũ��Ϊc��Ag+��=![]() =
=![]() =1
=1![]() 10-5��mol/L��
10-5��mol/L��![]() 1.8
1.8![]() 10-8��mol/L����Cl-�ȳ�����C�����D��Ag2CrO4��s��+2Cl-
10-8��mol/L����Cl-�ȳ�����C�����D��Ag2CrO4��s��+2Cl-![]() 2AgCl��s��+CrO42-��aq����ƽ�ⳣ��K=
2AgCl��s��+CrO42-��aq����ƽ�ⳣ��K=![]() =
=![]() =
=![]() =1.0
=1.0![]() 10-12
10-12![]() ��1.8
��1.8![]() 10-10��2=3.1
10-10��2=3.1![]() 107��D����ȷ����ѡD��
107��D����ȷ����ѡD��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(HCOOH)�ǻ�ԭ���ᣬ�ֳ������ᣬ��������ҽҩ��Ⱦ�ϡ�Ƥ��ȹ�ҵ������ij��ѧ��ȤС���ڷ����������ɺͽṹ�Լ����ijЩ���ʽ�����̽������ش��������⡣
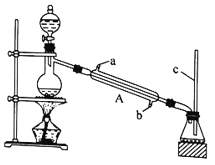
I.�������봼����������Ӧ
����ȤС��������ͼ��ʾװ�ý��м���(HCOOH)��״�(CH3OH)��������Ӧʵ��:
�й����ʵ���������:
�е�/�� | �ܶ�(g��cm-3) | ˮ���ܽ��� | |
�״� | 64.5 | 0.79 | ���� |
���� | 100.7 | 1.22 | ���� |
������� | 31.5 | 0.98 | ���� |
(1)װ���У�����A��������_________________����������c��������__________________________��
(2)����ͼ״�����������Ӧ�Ļ�ѧ����ʽΪ____________________________________________��
(3)Ҫ����ƿ�����õĻ��������ȡ����������ɲ��õķ���Ϊ__________________________________��
II.��������ˮ��ȡһ����̼

(1)������ͼװ���Ʊ����ռ�CO����������ȷ������˳��Ϊa��__________(�������������������Сд��ĸ��ʾ)��
(2)װ��B��������__________________________________��
(3)һ�������£�CO����NaOH���巢����Ӧ:CO+NaOH ![]() HCOONa��
HCOONa��
��Ϊ��֤����CO��NaOH���巢���˷�Ӧ����������ж���ʵ�鷽��:ȡ�����������Һ��___________��
���ⶨ�����м�����(HCOONa)�Ĵ�����ȷ��ȡ�������8,0g���Ƴ�100mL��Һ����ȡ20.00mL����Һ����ƿ�����ټ���___________��ָʾ������1.5mol/L���������Һ�ζ�ʣ���NaOH��ƽ�еζ����Σ�ƽ��������������Ϊ5.05mL��������м����Ƶ���������Ϊ_______(��������ȷ��0.1%)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ�д��ڶ��ַ��Ӻ����ӣ������ڲ�ͬ�ķ�Ӧ�б��ָ��Ե����ʣ�����ʵ������ͽ���һ������ȷ����
A. ������ɫ������һ�����ɫ������ɫ��˵����Һ����Cl2����
B. ��Һ�ʻ���ɫ�����д̼�����ζ��˵����HClO���Ӵ���
C. ����AgNO3��Һ������ɫ������˵����Cl-���Ӵ���
D. ����NaOH��Һ����ˮ����ɫ��ʧ��˵����HClO���Ӵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ܵĻ������ڴ��Բ���������������졢�����Ʊ��ȷ���ӦƬ�dz��㷺��
(1)Co2+��̬��Χ�����Ų�ʽΪ______________��
(2)�Ʊ�[Co(H2O)6]2+��ӦΪ(NH4)2[Co(SCN)4]+6H2O=[Co(H2O)6](SCN)2+2NH4SCN��
�������[Co(H2O)6]2+����Co2+�γ���λ����ԭ����_______(��Ԫ�ط���)��SCN-�Ŀռ乹��Ϊ_____(����������)��
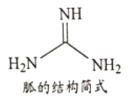
��NH4SCN��180-190��ֽⲢ�Ƶ���(�ṹ��ʽ����ͼ��ʾ)���ҷ����е�ԭ���ӻ��������____��lmol���к��Ҽ���ĿΪ___________��
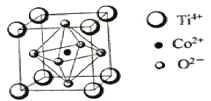
(3)һ���ܵĻ����������ʯ������Ĵ������侧���ṹ����ͼ��ʾ����������ÿ��O2-���ڵ�O2-��________��(������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������״����(COVID��19)��һ���²��Ժ�ǿ��RNA������ҽ�þƾ����������������������ᶼ�������ڼ�ͥ�������������ʵ���ɺ����ʽ��з��࣬����״��������
A.������B.����C.���D.����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���мס��������л���ṹ��ʽ����ͼ��������˵������ȷ����
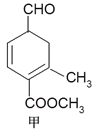
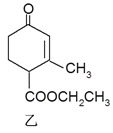
A. ���������CCl4��Һ�����ӳɷ�Ӧ������������ʵ����ֱ�Ϊ2mol��1mol
B. �ס��һ�Ϊͬ���칹��
C. 1mol����H2��һ�������·�Ӧ���������3mol H2
D. �����ʵ����ļס��ҷֱ���NaOH��Һ��Ӧ������NaOH������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и��������У�������ͬ����������ǣ� ��
A.���������ι�
B.̼�Ͷ�����̼
C.ľ̿�ͻ���̿
D.�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Կ��淴Ӧ4NH3��g��+ 5O2��g��![]() 4NO��g��+ 6H2O��g��������������ȷ���ǣ� ��
4NO��g��+ 6H2O��g��������������ȷ���ǣ� ��
A. �ﵽ��ѧƽ��ʱ��4������O2��= 5������NO ��
B. ����λʱ��������x mol NO��ͬʱ������x mol NH3 ����Ӧ�ﵽƽ��״̬
C. �ﵽ��ѧƽ��ʱ�����������������������Ӧ���ʼ��٣��淴Ӧ��������
D. ��ѧ��Ӧ���ʹ�ϵ�ǣ�2������NH3��= 3������H2O��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�����Һ������������������ķ����ǣ� ��
A.��ȡ
B.����
C.����
D.�����ЧӦ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com