
【题目】有机物F是一种香料,其合成路线如图所示:

已知:i、
ii、
(1)A的名称为_____,F中的含氧官能团为_____(写名称)
(2)B的分子式为 C7H7Cl,步骤I的反应试剂和条件为______。
(3)步骤Ⅱ反应的化学方程式为______,反应类型为______。
(4)满足括号中条件(①苯环上只有两个取代基②能与FeCl3溶液发生显色反应③能发生水解反应和银镜反应)的E的同分异构体有____种,其中核磁共振氢谱峰面积比为6:2:2:1:1的分子的结构简式为_____。
(5)依据题中信息,完成以![]() 为原料制取试剂X
为原料制取试剂X 的合成路线图(无机试剂一定要选银氨溶液,其它无机试剂任选)_______。
的合成路线图(无机试剂一定要选银氨溶液,其它无机试剂任选)_______。
合成路线图示例如下:CH2=CH2 ![]() CH3CH2Br
CH3CH2Br ![]() CH3CH2OH
CH3CH2OH
【答案】甲苯 醚键和酯基 氯气、光照 ![]() +NaOH
+NaOH![]()
 +NaCl 取代反应 15
+NaCl 取代反应 15 ![]()
![]()
【解析】
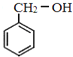
由A转化为![]() 可知A为甲苯,则A为
可知A为甲苯,则A为![]() ;由F的结构可知C、E分别为
;由F的结构可知C、E分别为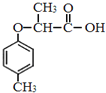 和
和 中的一种,结合转化可知,反应I是甲苯与氯气在光照条件下反应生成
中的一种,结合转化可知,反应I是甲苯与氯气在光照条件下反应生成![]() ,则B为
,则B为![]() ;
;![]() 在氢氧化钠溶液中共热水解反应生成
在氢氧化钠溶液中共热水解反应生成 ,则C为
,则C为 ;E为
;E为 ,结合信息可知一定条件下与氢氧化钠反应生成
,结合信息可知一定条件下与氢氧化钠反应生成 ,则D为
,则D为 ;
; 与CH3CHClCOOH反应生成
与CH3CHClCOOH反应生成 ,则X为CH3CHClCOOH。
,则X为CH3CHClCOOH。
(1)A的结构简式为![]() ,名称为甲苯;F的结构简式为
,名称为甲苯;F的结构简式为 ,含有的官能团为醚键和酯基,故答案为:甲苯;醚键和酯基;
,含有的官能团为醚键和酯基,故答案为:甲苯;醚键和酯基;
(2)步骤I是甲苯与氯气在光照条件下反应生成![]() ,故答案为:氯气、光照;
,故答案为:氯气、光照;
(3)步骤Ⅱ为![]() 在氢氧化钠溶液中共热水解反应生成
在氢氧化钠溶液中共热水解反应生成![]() ,反应的化学方程式
,反应的化学方程式![]() +NaOH
+NaOH![]()
 +NaCl,故答案为:
+NaCl,故答案为:![]() +NaOH
+NaOH![]()
 +NaCl;取代反应;
+NaCl;取代反应;
(4)E的结构简式为 ,其同分异构体符合苯环上只有两个取代基,能与FeCl3溶液发生显色反应,说明含有酚羟基,能发生水解反应和银镜反应,含有甲酸形成的酯基,其中一个为-OH,另外取代基为-CH2CH2CH2OOCH,或者-CH(CH3)CH2OOCH,或者为-CH2CH(CH3)OOCH,或者为-C(CH3)2OOCH,或者-CH(CH2CH3)OOCH,各有邻、间、对3种,故共有15种,其中核磁共振氢谱峰面积比为6:2:2:1:1的分子的结构简式为
,其同分异构体符合苯环上只有两个取代基,能与FeCl3溶液发生显色反应,说明含有酚羟基,能发生水解反应和银镜反应,含有甲酸形成的酯基,其中一个为-OH,另外取代基为-CH2CH2CH2OOCH,或者-CH(CH3)CH2OOCH,或者为-CH2CH(CH3)OOCH,或者为-C(CH3)2OOCH,或者-CH(CH2CH3)OOCH,各有邻、间、对3种,故共有15种,其中核磁共振氢谱峰面积比为6:2:2:1:1的分子的结构简式为![]() ,故答案为:15;
,故答案为:15; ![]() ;
;
(5)![]() 先发生催化氧化生成醛,再进一步氧化生成羧酸,最后与氯气、红磷作用得到
先发生催化氧化生成醛,再进一步氧化生成羧酸,最后与氯气、红磷作用得到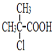 ,合成路线流程图为
,合成路线流程图为![]() ,故答案为:
,故答案为: ![]() 。
。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
【题目】表中原子化热、晶格能、键能的单位都是kJmol﹣1

则下列说法正确的是
A. Na(s)与Cl2(g)反应生成1mol NaCl(s)放出的热量为556.1kJ
B. Si(s)+2Cl2(g)═SiCl4(g)△H=﹣602kJmol﹣1
C. 从表中可以看出,氯化钠的熔点比晶体硅高
D. 从表中数据可以看出,微粒半径越大金属键、离子键越弱,而共价键却越强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 纤维素、花生油、蚕丝在一定条件下都能发生水解反应
B. 煤的干馏是化学变化,煤的气化、液化和石油的分馏都是物理变化
C. 新戊烷用系统命名法命名为2,2-二甲基戊烷
D. 正四面体烷(![]() )与立方烷(
)与立方烷(![]() )的二氯代物数目相同
)的二氯代物数目相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:CO(g)+ 2H2(g)![]() CH3OH(g) △H
CH3OH(g) △H
(1)已知CO(g)、H2(g)的标准燃烧热分别为-285.8kJmol-1,-283.0kJmol-1,且CH3OH(g)+3/2O2(g)![]() CO2(g)+2H2O(l) △H=-761 kJmol-1;则CO(g)+ 2H2(g)
CO2(g)+2H2O(l) △H=-761 kJmol-1;则CO(g)+ 2H2(g)![]() CH3OH(g)的△H= ___________。
CH3OH(g)的△H= ___________。
(2)反应的ΔS_______0(填“>”、“<”或“=”)。在________(填“较高”或“较低”)温度下该反应自发进行。
(3)若将等物质的量的CO和H2混合气体充入恒温恒容密闭容器中进行上述反应,下列事实能说明此反应已达到平衡状态的是_______________。
A.容器内气体密度保持不变 B.混合气体的平均相对分子质量不变
C.生成CH3OH的速率与生成H2的速率相等 D.CO的体积分数保持不变
(4)下图中能正确反映平衡常数K随温度变化关系的曲线为__________(用a或b表示)。

(5)投料比n(H2)/n(CO)=2时,体系中CO的平衡转化率(α)温度和压强的关系如图2所示。α(CO)值随温度升高而___________(填“增大”或“减小”)其原因是___________________________;下图中的压强由大到小为__________________(用P1,P2,P3表示)。

(6)520K时, 投料比n(H2)/n(CO)=2(总物质的量为3mol),维持反应过程中压强P3不变,达到平衡时测得容器体积为0.1L,则平衡常数K=_______。若H2和CO的物质的量之比为n∶1(维持反应过程中压强P3不变),相应平衡体系中CH3OH的物质的量分数为x,请在下图中绘制x随n变化的示意图_______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见的太阳能电池有单晶硅或多晶硅太阳能电池、GaAs太阳能电池及铜铟镓硒薄膜太阳能电池等。请回答下列问题:
(1)基态硒原子的价电子排布式为___;H2O的沸点高于H2Se的沸点(-42℃),其原因是___。
(2)已知GaCl3晶体熔点为77.9℃,沸点为201.3℃,GaCl3品体类型为____。
(3)Na3AsO4中阴离子的空间构型为_____,As原子采取_____杂化。
(4)高温下CuO容易转化为Cu2O,试从原子结构角度解释原因:_____。
(5)锌与铜位于同一周期。硫化锌的晶胞结构如图所示,S2-周围等距离且最近的Zn2+个数为____;若晶胞边长为dpm,则硫化锌的密度为____g·cm-3(不必简化)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验、现象与结论正确且相符的是( )
实验 | 现象 | 结论 | |
A | 向盛有H2O2溶液的试管中加入几滴酸化的硫酸亚铁溶液 | 溶液变成棕黄色,一段时间后,溶液中出现气泡,随后有红褐色沉淀生成 | Fe2+催化H2O2分解产生O2;H2O2分解反应放热,促进Fe3+的水解平衡正向移动 |
B | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应: 2NO2 (g) |
C | SO2通入新制氯水 | 溶液褪色 | SO2具有漂白性 |
D | 向2支盛有2mL相同浓度硝酸银溶液的试管中,分别加入2滴相同浓度的NaCl和NaI溶液 | 一支无明显现象,另一支产生黄色沉淀 | 相同条件下,AgI比AgCl的溶解度大 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锡酸钠用于制造陶瓷电容器的基体、颜料和催化剂。以锡锑渣(主要含Sn、Sb、As、Pb的氧化物)为原料,制备锡酸钠的工艺流程图如下:

请回答下列问题:
(1)Sn(ⅣA)、As(VA)、Sb(VA)三种元素中,As和Sb最高正化合价为___________,Sn的原子序数为50,其原子结构示意图为___________。
(2)从溶液中得到锡酸钠晶体的实验操作是___________、趁热过滤、干燥。
(3)“碱浸”时,若SnO含量较高,工业上则加入NaNO3,其作用是______________________;如图是“碱浸”实验的参数,请选择“碱浸”的合适条件_________________________________。

(4)“脱铅”是从含Na2PbO2的溶液中形成硫化铅渣,其离子方程式为_________________。
(5)“脱锑”时发生的化学方程式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下说法正确的是 ( )
A. 同分异构体之间分子式相同,其式量也一定相等,式量相等的物质一定是同分异构体。
B. 同分异构体之间某种元素的质量分数均相同,化合物之间某种元素质量分数均相同的物质一定为同分异构体。
C. 两种物质如果互为同分异构体,则一定不可能为同系物。
D. 互为同分异构体的物质之间物理性质一定不同,但化学性质一定相似。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,关于pH=11的NH3·H2O溶液,下列分析正确的是
A. c(NH3·H2O)=10-3mol/L
B. 由水电离出的c(H+)=10-11 mol/L
C. 加入少量 NH4Cl固体,NH3·H2O的电离平衡逆向移动,KW值减小
D. 加入等体积 pH=3的盐酸,所得溶液:c(Cl-)>c(NH4+)>c(H+)>c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com