
下列实验过程中产生的现象与如图所示座标图形相符合的是()
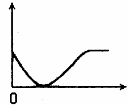
A. 稀盐酸滴加到一定量NaHCO3,溶液中(横坐标是稀盐酸的体积,纵坐标为气体体积)
B. NaOH溶液滴入Ba(HCO3)2溶液中(横坐标是NaOH溶液的体积,纵坐标为沉淀质量)
C. 稀盐酸滴加到AgNO3溶液中(横坐标是稀盐酸的体积,纵坐标为溶液的导电能力)
D. 稀硫酸滴加到Ba(OH)2溶液中(横坐标是稀硫酸的体积,纵坐标为溶液的导电能力)
考点: 酸碱混合时的定性判断及有关ph的计算;电解质溶液的导电性.
专题: 离子反应专题.
分析: A.稀盐酸滴加到一定量NaHCO3溶液中发生NaHCO3+HCl=NaCl+CO2↑+H2O;
B.NaOH溶液滴入Ba(HCO3)2溶液中发生HCO3﹣+OH﹣=CO32﹣+H2O,CO32﹣+Ba2+=BaCO3↓;
C.稀盐酸滴加到AgNO3溶液中发生HCl+AgNO3=HNO3+AgCl↓;
D.稀硫酸滴加到Ba(OH)2溶液中发生Ba(OH)2+H2SO4═BaSO4↓+2H2O,根据反应的化学方程式或离子方程式判断.
解答: 解:A.稀盐酸滴加到一定量NaHCO3溶液中发生NaHCO3+HCl=NaCl+CO2↑+H2O,随着盐酸的滴加,生成二氧化碳气体逐渐增多,故A错误;
B.NaOH溶液滴入Ba(HCO3)2溶液中发生HCO3﹣+OH﹣=CO32﹣+H2O,CO32﹣+Ba2+=BaCO3↓,沉淀质量逐渐增大,不可能先减小再增大,故B错误;
C.如是等浓度,稀盐酸滴加到AgNO3溶液中发生HCl+AgNO3=HNO3+AgCl↓,溶液离子物质的量不变,但浓度逐渐减小,不可能增大,故C错误;
D.滴入的硫酸与氢氧化钡反应,生成硫酸钡沉淀和水,溶液中离子浓度减少,导电能力下降,恰好完全反应导电性变为零,再随着稀硫酸的滴入,溶液导电能力增加,直到变为定值,故D正确;
故选D.
点评: 本题考查了化学反应及图象的关系,较为综合,解题的重点是能正确分析变化过程,读懂图象并与反应相结合是解题的关键,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
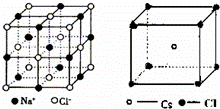
认真分析NaCl和CsCl的晶体结构,判断下列说法错误的是( )
|
| A. | NaCl和CsCl都属于AB型的离子晶体 |
|
| B. | NaCl和CsCl晶体中阴、阳离子个数比相同,所以阴、阳离子的配位数相等 |
|
| C. | NaCl和CsCl晶体中阴、阳离子的配位数分别为6和8 |
|
| D. | NaCl和CsCl都属于AB型的离子晶体,所以阴、阳离子半径比相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是()
A. 能电离出H+的化合物叫做酸
B. 实验测得1mol某气体体积为22.4L,测定条件一定是标准状况
C. 摩尔是七个基本物理量之一
D. 用树状分类法可以将化合物分类为酸、碱、盐和氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
在某无色酸性溶液中能大量共存的一组离子是()
A. NH4+、SO42﹣、Al3+、NO3﹣ B. Na+、K+、HCO3﹣、NO3﹣
C. Na+、Ca2+、NO3﹣、CO32﹣ D. K+、Cu2+、NH4+、NO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
请完成下列填空:
(1)同温同压下等体积的SO2和SO3中,所含原子数之比为 .
(2)中和100mL 0.1mol/L的稀硫酸,需NaOH的质量为
(3)现有m g某气体,它由双原子分子构成,它的摩尔质量为M g•mol﹣1,则:
①该气体在标准状况下的体积为
②该气体溶于水后形成V L溶液(不考虑反应),其溶液的物质的量浓度 L﹣1.
查看答案和解析>>
科目:高中化学 来源: 题型:
某实验兴趣小组按如图装置实验后,所记录内容合理的是()
实验
记录 ①Cu为正极,Zn为负极;
②Zn质量减少,Cu质量不变;
③SO42﹣ 向Cu极移动;
④电子流方向是:由Zn经导线流入Cu片;
⑤Zn电极发生还原反应;
⑥正极反应式:Cu2++2e﹣═Cu

A. ①④⑥ B. ②③④ C. ①②⑤ D. ③⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com