
分析 热化学方程式中,焓变数值与化学计量数成正比;焓变为负值,放热热量越大,焓变值越小,据此进行解答.
解答 解:已知:
①H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H1=akJ•mol-1
②2H2(g)+O2(g)═2H2O(g)△H2=bkJ•mol-1
③H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H3=ckJ•mol-1
④2H2(g)+O2(g)═2H2O(l)△H4=dkJ•mol-1,
反应①③的计量数小于②④,则反应①②放出热量小于②④,而焓变为负值,则a、c大于b、d;
反应①③、②④,气态水具有能量大于液态水,则反应①放热热量小于③,反应②放出热量小于反应④,焓变为负值,则a>c、b>d,
所以a、b、c、d间的大小关系为:a>c>b>d,
故答案为:a>c>b>d.
点评 本题考查了反应热大小比较,题目难度不大,明确反应热与焓变的关系为解答关键,试题侧重基础知识的考查,有利于提高学生的灵活应用能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
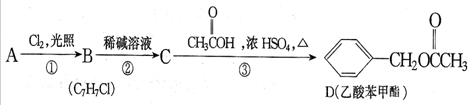
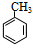 .
.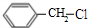 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$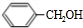 +NaCl.
+NaCl.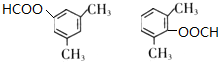 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
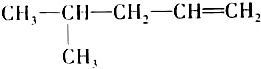
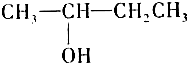
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al具有良好延展性和抗腐蚀性,可制成铝箔包装物品 | |
| B. | NaHCO3能与碱反应,食品工业用作焙制糕点的膨松剂 | |
| C. | 药皂中加入少量苯酚,可以起到杀菌消毒的作用 | |
| D. | 明矾能水解生成Al(OH)3胶体,可用作净水剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 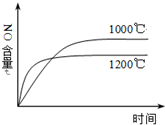 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-a kJ•mol-1 | |
| B. | 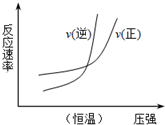 N2(g)+3H2(g)?2NH3(g)△H=+b kJ•mol-1 | |
| C. | 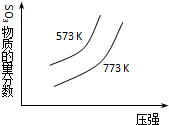 2SO2(g)+O2(g)?2SO3(g)△H=+C kJ•mol-1 | |
| D. | 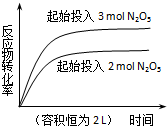 2N2O5(g)?4NO2(g)+O2(g)△H=+d kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
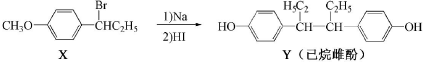
| A. | 在NaOH水溶液中加热,化合物X可发生消去反应 | |
| B. | 在一定条件,化合物Y可与HCHO发生缩聚反应 | |
| C. | 该反应为消去反应 | |
| D. | 化合物X中肯定有9个C原子共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用瓷坩埚熔融氢氧化钠或碳酸钠 | |
| B. | 用玻璃棒蘸取溶液,点在湿润的pH试纸上测定溶液的pH值 | |
| C. | 取用金属钠、钾时,未用完的钠、钾应放回原瓶 | |
| D. | 读取量筒内液体的体积,俯视读数会导致读数偏小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入氧气的一极为正极,发生氧化反应 | |
| B. | 该电池负极的电极反应为2H2-4e-=4H+ | |
| C. | 该电池工作一段时间,电解质溶液浓度保持不变 | |
| D. | 该电池在工作时,溶液中的阴离子向负极移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com