
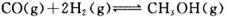 的化学平衡常
的化学平衡常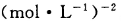 。
。
 H2↑+Cl2↑+2OH?(2分)
H2↑+Cl2↑+2OH?(2分) H++Cl?+HClO,增大H+浓度使平衡逆向移动,减少Cl2在水中的溶解,有利于Cl2逸出。(2分)
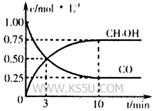
H++Cl?+HClO,增大H+浓度使平衡逆向移动,减少Cl2在水中的溶解,有利于Cl2逸出。(2分) CH3OH(g)
CH3OH(g) H2↑+Cl2↑+2OH?
H2↑+Cl2↑+2OH? H++Cl?+HClO,加入盐酸控制阳极区溶液的pH在2~3,增大H+浓度使平衡逆向移动,减少Cl2在水中的溶解,有利于Cl2逸出。
H++Cl?+HClO,加入盐酸控制阳极区溶液的pH在2~3,增大H+浓度使平衡逆向移动,减少Cl2在水中的溶解,有利于Cl2逸出。

 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源:不详 题型:单选题
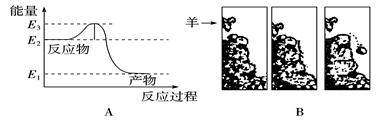
| A.E2 | B.E2-E1 | C.E3-E2 | D.E3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
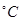 时,在2L的恒容密闭容器中充入2molNO和1molO2发生反应,2NO(g)+O2(g)
时,在2L的恒容密闭容器中充入2molNO和1molO2发生反应,2NO(g)+O2(g) 2NO2(g),经5min达到平衡,测得c(NO)="0.5" mol/L,并放热QkJ。5min内 v(O2)=___________。
2NO2(g),经5min达到平衡,测得c(NO)="0.5" mol/L,并放热QkJ。5min内 v(O2)=___________。 2NO2(g)的△H= 。
2NO2(g)的△H= 。查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
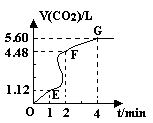 (气体体积均在标准状况下测定)。请回答下列问题:
(气体体积均在标准状况下测定)。请回答下列问题:| A.蒸馏水 | B.氯化钾固体 | C.氯化钠溶液 | D.浓盐酸 |
 (3)加入CaCO3的质量为 。
(3)加入CaCO3的质量为 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
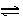 2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为
2NH3,在2L密闭容器中进行,5min内氨的质量增加了1.7g,则反应速率为| A.v(H2)=0.03mol/(L·min) | B.v(N2)="0.005mol/(L·min)" |
| C.v(NH3)=0.17mol/(L·min) | D.v(NH3)=0.02mol/(L·min) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
 SO2(g)+Cl2(g) △H=+97.3 kJ·mol-1。某温度时向体积为1 L的恒容密闭容器中充入0. 20mol SO2Cl2,达到平衡时,容器中含0.18mol SO2,则此过程反应吸收的热量为_____ kJ,该温度时反应的平衡常数为_____。将上述所得混合气体溶于足量BaCl2溶液中,最终生成沉淀的质量为_______。
SO2(g)+Cl2(g) △H=+97.3 kJ·mol-1。某温度时向体积为1 L的恒容密闭容器中充入0. 20mol SO2Cl2,达到平衡时,容器中含0.18mol SO2,则此过程反应吸收的热量为_____ kJ,该温度时反应的平衡常数为_____。将上述所得混合气体溶于足量BaCl2溶液中,最终生成沉淀的质量为_______。 2SO3(g) △H=-198kJ·mol-1,400℃,1.01×105Pa,向容积为2L的恒容密闭容器中充入一定量 SO2和O2,n(SO3)和n(O2)随时间的变化曲线如图所示。
2SO3(g) △H=-198kJ·mol-1,400℃,1.01×105Pa,向容积为2L的恒容密闭容器中充入一定量 SO2和O2,n(SO3)和n(O2)随时间的变化曲线如图所示。
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
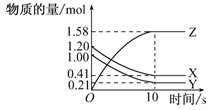
| A.从反应开始到10 s末,用Z表示的反应速率为0.158 mol/(L·s) |
| B.从反应开始到10 s末,用X表示的反应速率为0.79 mol/(L·s) |
| C.从反应开始到10 s末,Y的转化率为79.0% |
| D.该反应的化学方程式为X(g)+Y(g)=Z(g) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
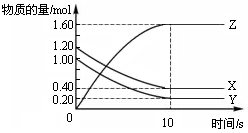
| A.前10s内 v(X)=0.08mol·L-1·s-1 |
| B.该反应的平衡常数K= 4 |
| C.平衡时X、Y的转化率相同 |
| D.达到平衡后,将容器体积扩大为 4 L,平衡向逆反应方向移动 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com