
����Ŀ��2����1��3�������ɼ䱽�����Ȼǻ�������������ȥ��������ɡ�ԭ�����£�
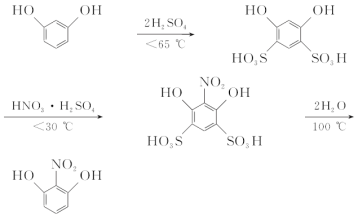
�������ʵ�����������£�
���� | ��Է������� | ��״ | �۵�/�� | ˮ����(����) |
�䱽���� | 110 | ��ɫ��״���� | 110.7 | ���� |
2����1��3������ | 155 | �ۺ�ɫ��״���� | 87.8 | ���� |
�Ʊ��������£�
��һ�����ǻ�����ȡ71.5g�䱽���ӣ���ɷ�ĩ������ƿ�У�������������Ũ���Ტ���Ͻ��裬�����¶���һ����Χ��15min(��ͼ1)��
�ڶ��������������ǻ���Ӧ��������ƿ������ˮ�У������ȴ��������������������¶ȼ�������15min��
������������������Ӧ������ϡ��Һת�Ƶ�Բ����ƿB�У�Ȼ����ͼ2��ʾװ�ý���ˮ��������(ˮ���������ʹ���ᴿ���л����ڵ���100����������ˮ����һ������������Ӷ��ﵽ�����ᴿ��Ŀ��)��
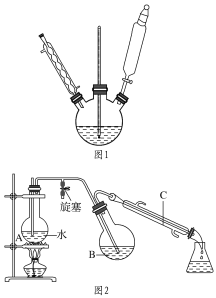
��ش��������⣺
��1���ǻ������п����¶�����ʵķ�ΧΪ(����ĸ)__��
a.30�桫60�� b.60�桫65�� c.65�桫70�� d.70�桫100��
��2��ͼ2�е��������Ƿ���Ի�Ϊͼ1����������___����������������������
��3��������������ȡ���������ľ��������__��
��4��ͼ2�У���ƿA�г�����������ѹ���ã����ܷ�ֹװ����ѹǿ���������¹ʣ����ܷ�ֹ__��������C�п��ܿ�����������__����Ӧһ��ʱ���ֹͣ����ʱ�IJ�����__(���й������;ƾ��ƵIJ���)��
��5��ˮ���������Ƿ�����ᴿ�л���ķ���֮һ�����ᴿ���ʱ���߱���������ȷ����__��
a.���ܻ�������ˮ������������
b.�ڷ�������ˮ��������ѧ��Ӧ
c.�ѻӷ���
d.������ˮ
��6����ʵ�����ջ��12.0g�ۺ�ɫ���壬��2����1��3�����ӵIJ���ԼΪ__��������3λ��Ч���֣�
���𰸡�b �� ���ձ��м���������Ũ���ᣬ�ر��ڻ�������һ������Ũ���ᣬ�ӱ߽��裬��ȴ ѹǿ��С������ �������ڱ��нۺ�ɫ�������� ����������ȥ�ƾ��� ab 11.9%
��������
��1��Ϊ�����ʵ��ķ�Ӧ���ʼ���ֹ��������֣���Ӧ�¶�һ�������60��65�����ң�
��2����ͼ2�е�ֱ�������ܻ�Ϊͼ1���õ����������ܣ������ڱ�������Һ��˳�����£�
��4��ͼ2�У���ƿA�г�����������ѹ���ã����ܷ�ֹװ����ѹǿ���������¹ʣ����ܷ�ֹѹǿ��С�������������ݷ�Ӧԭ������ֱ��������C��Ӧ����2-����-1��3-�����ӣ�����ȴ���Թ�����ʽ���֣��ݴ��ж�����ֹͣ����ʱ��Ӧ�ȴ�������ֹͣ��A�����ȣ�
��5������ˮ����������������ᴿ���ʣ����ᴿ���ʱ��벻�ܻ�������ˮ�����������롢�ڷ�������ˮ��������ѧ��Ӧ������һ���Ļӷ��ԣ��ݴ�ѡ��
��6�����ݲ��ʹ�ʽ����ɵá�
��1���������֪��Ϊ�����ʵ��ķ�Ӧ���ʼ���ֹ��������֣���Ӧ�¶�Ӧ������60��65�����ң�b��ȷ���ʴ�Ϊ��b��
��2����ͼ2�е�ֱ�������ܻ�Ϊͼ1���õ����������ܣ������ڱ�������Һ��˳�����£��ʴ�Ϊ����
��3����Һ���ʱ��������ܶȴ����Һ���뵽�ܶ�С����Һ�У�Ũ������ܶȴ���Ũ���ᣬ��������������ȡ�����ᡱ�ľ������������ƿ�м�������Ũ���ᣬ�ر��ڻ�������һ������Ũ���ᣬ�ӱ߽��裬��ȴ���ʴ�Ϊ�����ձ��м���������Ũ���ᣬ�ر��ڻ�������һ������Ũ���ᣬ�ӱ߽��裬��ȴ��
��4��ͼ2�У���ƿA�г�����������ѹ���ã����ܷ�ֹװ����ѹǿ���������¹ʣ����ܷ�ֹѹǿ��С�������������ݷ�Ӧԭ������ֱ��������C��Ӧ����2-����-1��3-�����ӣ�����ȴ���Թ�����ʽ���֣�����Թ۲쵽�������ڱ��нۺ�ɫ����������ֹͣ����ʱ��Ӧ�ȴ�������ֹͣ��A�����ȣ��ʴ�Ϊ����ֹѹǿ��С�����������нۺ�ɫ�����������ȴ������ٳ�ȥ�ƾ��ƣ�
��5������ˮ����������������ᴿ���ʣ����ᴿ���ʱ��벻�ܻ�������ˮ�����������롢�ڷ�������ˮ��������ѧ��Ӧ������һ���Ļӷ��ԣ���ab��ȷ���ʴ�Ϊ��ab��
��6��71.5g�䱽���ӵ����ʵ���Ϊ0.65mol������Ԫ���غ��֪�����ɵ�2-����-1��3-�����ӵ�����Ϊ0.65mol��155g/mol=100.75g����2����1��3�����ӵIJ���Ϊ![]() ��100%=11.9%���ʴ�Ϊ��11.9%��
��100%=11.9%���ʴ�Ϊ��11.9%��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ѧ��ӦA2(g)+B2(g)��2AB(g)�������仯��ͼ��ʾ���ж�������������ȷ���ǣ� ��
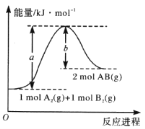
A. ÿ����2 mol AB����bkJ����
B. �÷�Ӧ����H= + (a-b)kJ mol-1
C. �÷�Ӧ�з�Ӧ��������������������������
D. ����1 mol A��A��1 mol B��B�����ų�akJ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͭ�ǹ㷺Ӧ�������������Ԫ�������úϽ�ij����С���ij����ͭԪ��(��25%BeO��71%CuS������FeS��SiO2)�л������ͭ���ֽ����Ĺ���������ͼ��

��֪����.�롢��Ԫ�صĻ�ѧ�������ƣ�������������������Һ��Ӧ���ɿ�����ˮ��Na2BeO2
��.�����²�����������ܶȻ��������±���
������ | Cu(OH)2 | Fe(OH)3 | Mn(OH)2 |
�ܶȻ�����(Ksp) | 2.2��10-20 | 4.0��10-38 | 2.1��10-13 |
��1����ҺA����Ҫ�ɷֳ�NaOH�⣬����__(�ѧʽ)��д����ӦI�к��뻯������������ᷴӦ�����ӷ���ʽ��__��
(2)����ҺC�к�NaCl��BeCl2������HCl��Ϊ�ᴿBeCl2���������ʵ�鲽��˳��Ϊ__(����ĸ)��
a.��������İ�ˮ b.ͨ�������CO2 c.���������NaOH d.����������HCl e.ϴ�� f.����
�ڴ�BeCl2��Һ�еõ�BeCl2����IJ�����__��
��3����MnO2�ܽ����������е���Ԫ������Ϊ���ʡ�д����Ӧ����CuS������Ӧ�Ļ�ѧ����ʽ��__��
������ŨHNO3�ܽ�������ȱ����__(��дһ��)��
��4����ҺD��c(Cu2+)=2.2mol��L-1��c(Fe3+)=0.008mol��L-1��c(Mn2+)=0.01mol��L-1����μ���ϡ��ˮ����pH�ɽ������η��룬���ȳ�������__(�����ӷ���)��Ϊʹͭ���ӿ�ʼ������������Ӧ������Һ��pH����__��
��5�����NaCl��BeCl2������ο��Ʊ������룬��ͼ�ǵ��װ��ͼ��

��ʯī�缫�ϵĵ缫��ӦʽΪ__��
�ڵ��õ���Be������Լ��1%��Na������ȥBe������Na�ķ���Ϊ__��
��֪�������ʵ��ۡ��е����±���
���� | �۵�(K) | �е�(K) |
Be | 1551 | 3243 |
Na | 370 | 1156 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��0.2 molij��A�������г��ȼ�պ����ɻ�����B��C��1.2 mol���Իش�
(1)��A�ķ���ʽΪ______________��
(2)��ȡһ��������A��ȫȼ�պ�����B��C��3 mol������______g��A�μ��˷�Ӧ��ȼ��ʱ��������______Ħ����
(3)����A����ʹ��ˮ��ɫ������һ�������£�������������ȡ����Ӧ����һ�ȴ���ֻ��һ�֣�����A�Ľṹ��ʽΪ______________��
(4)����A��ʹ��ˮ��ɫ���ڴ��������£���H2�ӳɣ���ӳɲ�������к���4��������A�����еĽṹ��ʽΪ____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������½�0.1mol��L-1���ռ���Һ���ϵμӵ�10.00mL��ͬŨ�ȵ�HA��Һ�У���Һ��-lgcˮ(H+)��NaOH��Һ�������ϵ��ͼ��ʾ[ע��cˮ(H+)Ϊ��Һ��ˮ�����c(H+)]������˵������ȷ���ǣ� ��
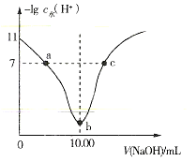
A.a��c������Һ�о����ڣ�c(H+)+c(Na+)=c(OH-)+c(A-)
B.b����Һ�д��ڣ�c(H+)+c(HA)=c(OH-)
C.a��b��c������Һ�У�b����Һ��������ǿ
D.0.1mol��L-1HA��Һ��HA�ĵ����ԼΪ1%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й���ѧ���ںϳɰ���N2+3H2![]() 2NH3��H<0����Ӧ�����о���ȡ���½�չ���״α�����LiH-3d���ɽ�����һ���ϴ�����ϵ�������������ת��������������ͼ��ʾ������˵������ȷ����
2NH3��H<0����Ӧ�����о���ȡ���½�չ���״α�����LiH-3d���ɽ�����һ���ϴ�����ϵ�������������ת��������������ͼ��ʾ������˵������ȷ����
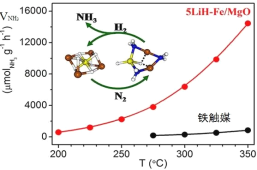
A.ת���������зǼ��Լ��������γ�
B.���ϴ��������˷�Ӧ�Ļ��
C.���ϴ����ܽ��ͺϳɰ���Ӧ���ʱ�
D.�����ºϳɰ��������ԭ��ת����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧ�ҷ���������ԭʼ�����е�COS���ʻ������������γɶ��ĵķ�Ӧ�д����ã���������Դ����Ҫ���á�
��1��д��COS�ĵ���ʽ________��C��O�γɹ��ۼ�ʱ,���õ��ӶԻ�ƫ��____ԭ�ӣ��ж�������___________��
��2����֪ COS��g��+ H2O��g��![]() H2S��g��+ CO2��g���� ��H1 = - 34kJ/mol
H2S��g��+ CO2��g���� ��H1 = - 34kJ/mol
CO��g��+ H2O��g��![]() H2��g��+ CO2��g���� ��H2 = - 41kJ/mol
H2��g��+ CO2��g���� ��H2 = - 41kJ/mol
д��H2S��CO��Ӧ���� COS ���Ȼ�ѧ����ʽ��_________��100�� ʱ��CO��H2S�����ʵ�����Ϊ 1:1 ���뷴Ӧ����,��ƽ���CO��ת������ = 33.3%����ʱ��Ӧ��ƽ�ⳣ��K =______��
��3���ڳ��д����ĺ�ѹ�ܱ������н��з�Ӧ�� ����ʼ����� n��CO��:n��H2S��=m����ͬʱ���ڲ��H2Sת������m���¶ȣ�T���Ĺ�ϵ��ͼ��ʾ��
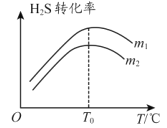
��m1________m2����� �� ������ �� ���� = ����
���¶ȸ��� T0ʱ��H2S ת���ʼ�С�Ŀ���ԭ��Ϊ________��
A ��Ӧֹͣ��
B ��Ӧ�� ��H ���
C ��Ӧ�ﵽƽ��
D �������Խ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������CO��H2�ڴ����������ºϳɼ״��������ķ�Ӧ���£�CO(g)+2H2(g)![]() CH3OH(g)�������һ�����ܱ������а����ʵ���֮��1��2����CO��H2�����ƽ��������CH3OH����������ڲ�ͬѹǿ�����¶ȵı仯��ͼ��ʾ������˵����ȷ����
CH3OH(g)�������һ�����ܱ������а����ʵ���֮��1��2����CO��H2�����ƽ��������CH3OH����������ڲ�ͬѹǿ�����¶ȵı仯��ͼ��ʾ������˵����ȷ����

A. �÷�Ӧ����H��0����p1��p2
B. ��Ӧ���ʣ�����(״̬A)������(״̬B)
C. ��C��ʱ��COת����Ϊ75%
D. �ں��º�ѹ���������ܱ������г��벻ͬ����CH3OH����ƽ��ʱCH3OH���������Ҳ��ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������װ���ܴﵽʵ��Ŀ�ĵ���( )
A.̽��AgCl��AgI֮���ת�� 
B.�Ƚ�Cl2��Br2��I2��������ǿ�� ![]()
C.�Ʊ�Fe(OH)2 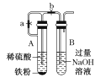
D.����֪Ũ�ȵ�����������Һ�ⶨ����Ũ�ȵ�ʵ�� 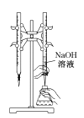
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com