
【题目】闪电时空气中有臭氧生成。下列说法正确的是( )
A.![]() 和
和![]() 互为同位素
互为同位素
B.![]() 与
与![]() 的相互转变是物理变化
的相互转变是物理变化
C.相同状况下,等体积![]() 和
和![]() 含有相同质子数
含有相同质子数
D.![]() 比
比![]() 氧化性更强
氧化性更强
【答案】D
【解析】
A.同种元素组成的不同单质为元素的同素异形体,同位素是质子数相同中子数不同的同种元素的不同原子;
B.同素异形体间的转化过程中结构发生改变是化学变化;
C.同温同压下,等体积的O2和O3含有相同的物质的量;
D.臭氧比氧气更活泼,氧化性更强.
A. 因O3和O2是由氧元素元素形成的不同单质,两者互为同素异形体,故A错误;
B. 因氧气与臭氧结构不同是不同的物质,其转化属于化学变化,故B错误;
C. 同温同压下,等体积的O2和O3含有相同的物质的量,所含氧原子数不同,质子数不同,故C错误;
D. 因臭氧比氧气更活泼,所以O2比O3稳定,O3比O2氧化性更强,故D正确;
故选D.


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】25 ℃时,在25 mL 0.1 mol·L-1的NaOH溶液中,逐滴加入0.2 mol·L-1的CH3COOH溶液,溶液的pH与醋酸体积关系如图,下列分析正确的是( )

A. B点的横坐标a=12.5
B. C点时溶液中有:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
C. D点时溶液中有:c(CH3COO-)+c(CH3COOH)=2c(Na+)
D. 曲线上A、B间的任意一点,溶液中都有:c(CH3COO-)>c(Na+)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解饱和食盐水是一项重要的化学工业,请完成下列计算:
(1)当电解产生0.2molNaOH时,能收集到标准状况下的H2____L。
(2)已知室温时饱和食盐水的溶质质量分数为0.265,取200g饱和食盐水进行电解,当NaCl反应了一半时停止电解,
①求出所得混合溶液中NaCl的质量。_____
②求出所得混合溶液中NaOH的质量分数。____(写出计算过程,保留3位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上合成乳酸(![]() )的一种途径如下:
)的一种途径如下:
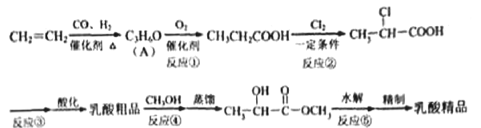
完成下列填空:
(1) 乳酸中的官能团名称是___________ 。A 的结构简式是___________。
(2)反应②的反应类型是___________。反应③的条件是___________。
(3)反应④的化学方程式为____________________________________________。
(4)聚乳酸是一种常用的可降解塑料,由乳酸聚合得到,其结构如下:

聚乳酸降解时,会产生自催化效应(降解的速度会越来越快) ,请解释原因__________。
(5)设计一条由丙烯制备丙酸的合成路线 _____________________ 。
(合成路线常用的表示方式为:A ![]() B ... ...
B ... ... ![]() 目标产物)
目标产物)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】![]() 是一种常见的强氧化剂,主要用于防腐、化工、制药等。现以某种软锰矿
是一种常见的强氧化剂,主要用于防腐、化工、制药等。现以某种软锰矿![]() 主要成分
主要成分![]() ,还有
,还有![]() 、
、![]() 、
、![]() 等
等![]() 作脱硫剂,通过如下简化流程既脱除燃煤尾气中的
作脱硫剂,通过如下简化流程既脱除燃煤尾气中的![]() ,又制得
,又制得![]() 反应条件已经省略
反应条件已经省略![]() 。
。
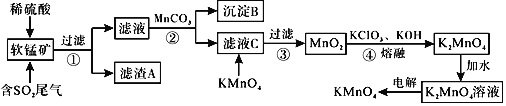
已知:![]() ,
,![]() 回答下列问题:
回答下列问题:
![]() 滤渣A的成分是
滤渣A的成分是![]() 写化学式
写化学式![]() ______。
______。
![]() 析出沉淀B时,首先析出的物质是
析出沉淀B时,首先析出的物质是![]() 写化学式
写化学式![]() ______。
______。
![]() 步骤2中加入
步骤2中加入![]() 的作用为______。
的作用为______。
![]() 滤液C中加入
滤液C中加入![]() 时发生反应的离子方程式是______。
时发生反应的离子方程式是______。
![]() 完成步骤4中反应的化学方程式______
完成步骤4中反应的化学方程式______![]() ______
______![]() ______
______![]() ______
______
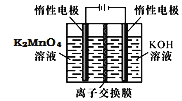
![]() 电解制备
电解制备![]() 的装置如图所示。电解液中最好选择______离子交换膜
的装置如图所示。电解液中最好选择______离子交换膜![]() 填“阳”或“阴”
填“阳”或“阴”![]() 。电解时,阳极的电极反应式为______。
。电解时,阳极的电极反应式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知高能锂离子电池的总反应式为2Li+FeS=Fe+Li2S,LiPF6·SO(CH3)2为电解质,用该电池为电源电解含镍酸性废水并得到单质Ni的实验装置如图所示。下列说法不正确的是

A. 电极Y为Li
B. 电解过程中,b中NaCl溶液的物质的量浓度将不断减小
C. X极反应式为FeS+2Li++2e-=Fe+Li2S
D. 若将图中阳离子膜去掉,将a、b两室合并,则电解反应总方程式发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在25 ℃、101 kPa下,1 g C8H18(辛烷)燃烧生成二氧化碳和液态水放出48.40 kJ热量,表示上述反应的热化学方程式正确的是( )
A. C8H18(l) + O2(g)![]() 8CO2(g) + 9H2O(l) ΔH=-48.40 kJ·mol-1
8CO2(g) + 9H2O(l) ΔH=-48.40 kJ·mol-1
B. C8H18(l) + O2(g)![]() 8CO2(g) + 9H2O(l) ΔH=-5 518 kJ·mol-1
8CO2(g) + 9H2O(l) ΔH=-5 518 kJ·mol-1
C. C8H18(l) + O2(g)![]() 8CO2(g) + 9H2O(l) ΔH=+5 518 kJ·mol-1
8CO2(g) + 9H2O(l) ΔH=+5 518 kJ·mol-1
D. C8H18(l) + O2(g)![]() 8CO2(g) + 9H2O(l) ΔH=+48.40 kJ·mol-1
8CO2(g) + 9H2O(l) ΔH=+48.40 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z为1~18号元素内除稀有气体外的4种元素,它们的原子序数依次增大,其中只有Y为金属元素。Y和W的最外层电子数相等。Y、Z两元素原子的质子数之和为W、X两元素质子数之和的3倍。
(1)写出元素符号:W为____,X为____,Y为____,Z为____。
(2)X的原子结构示意图为__________,Y___________(填“得到”或“失去”)电子时,形成的离子结构示意图为________________;Z得到电子,形成的阴离子的电子式为_____________.
(3)由X、Y、Z形成的一种化合物的电离方程式______________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】微量元素硼对植物生长及人体健康有着十分重要的作用,也广泛应用于新型材料的制备。
![]() 基态硼原子的价电子轨道表达式是______。与硼处于同周期且相邻的两种元素和硼的第一电离能由大到小的顺序为______。
基态硼原子的价电子轨道表达式是______。与硼处于同周期且相邻的两种元素和硼的第一电离能由大到小的顺序为______。
![]() 晶体硼单质的基本结构单元为正二十面体,其能自发地呈现多面体外形,这种性质称为晶体的______。
晶体硼单质的基本结构单元为正二十面体,其能自发地呈现多面体外形,这种性质称为晶体的______。
![]() 的简单氢化物
的简单氢化物![]() 不能游离存在,常倾向于形成较稳定的
不能游离存在,常倾向于形成较稳定的![]() 或与其他分子结合。
或与其他分子结合。
![]() 分子结构如图,则B原子的杂化方式为______。
分子结构如图,则B原子的杂化方式为______。

![]() 氨硼烷
氨硼烷![]() 被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是______,写出一种与氨硼烷互为等电子体的分子______
被认为是最具潜力的新型储氢材料之一,分子中存在配位键,提供孤电子对的成键原子是______,写出一种与氨硼烷互为等电子体的分子______![]() 填化学式
填化学式![]() 。
。
![]() 以硼酸
以硼酸![]() 为原料可制得硼氢化钠
为原料可制得硼氢化钠![]() ,它是有机合成中的重要还原剂。
,它是有机合成中的重要还原剂。![]() 的立体构
的立体构
型为______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com