
| ʵ�鲽�� | ʵ������ |
| �ٽ�þ����ɰֽ��ĥ�����Թ��У���������ˮ������ˮ���ڣ�������Һ�еμӷ�̪��Һ | A������ˮ���ϣ��۳�С���Ĵ��ζ���������˻˻��������֮��ʧ����Һ��ɺ�ɫ |
| �ڽ�һС������Ʒ�����з�̪��Һ����ˮ�� | B���������������Һ���dz��ɫ |
| �۽�þ��Ͷ��ϡ������ | C����Ӧ��ʮ�־��ң�������ɫ���� |
| �ܽ�����Ͷ��ϡ������ | D�����ҷ�Ӧ��Ѹ�ٲ���������ɫ���� |
| ʵ������ | �� | �� | �� | �� |
| ʵ��������A-D�� |
���� ��1���������ʵ������ж�ʵ������þ����ˮ��Ӧ���������������ݲ�������Ӧ����������þ����Һ�ʼ��ԣ��ƺ���ˮ��Ӧ�����������ƺ�������þ��Ͷ��ϡ�����У����ҷ�Ӧ��Ѹ�ٲ�����������������Ͷ��ϡ�����У���Ӧ��ʮ�־��ң�����������
��2��þ����ˮ��Ӧ����������������þ���ƺ���ˮ��Ӧ�����������ƺ��������ݴ˻ش�
��3������ʵ��������ʵ��Ŀ�ĵó����ۣ�
��� �⣺��1����þ����ɰֽ��ĥ�����Թ��У���������ˮ������ˮ���ڣ�þ����ˮ��Ӧ���������������ݲ�������Ӧ����������þ����Һ�ʼ��ԣ�������Һ�еμӷ�̪��Һ����Һ�ʺ�ɫ��
�����ƽϻ��ã�������з�̪��Һ����ˮ����Ϊ�����������ƶ�ʹ����Һ��ʾ��ɫ��ͬʱ������������������У�����ˮ���ϣ��۳�С���Ĵ��ζ���������˻˻��������֮��ʧ����Һ��ɺ�ɫ��
þ�������ã������������ᷢ���û���Ӧ����þ��Ͷ��ϡ�����У����ҷ�Ӧ��Ѹ�ٲ���������ɫ���壻
������Ͷ��ϡ�����У���Ӧ��ʮ�־��ң�������ɫ���壮
�ʴ�Ϊ��
| ʵ������ | �� | �� | �� | �� |
| ʵ������ | B | A | D | C |
���� ���⿼��ͬ����Ԫ�����ʵݱ���ɣ���Ŀ�Ѷ��еȣ�ע�����ʵ������Լ�Ԫ�������ɵĵݱ���ɣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��XY4������Xԭ�Ӵ���������������ģ���XY4����Ϊ�Ǽ��Է��� | |
| B�� | C2H5OH��C2H5Br��ȣ�ǰ�ߵ���Է�������ԶС�ں��ߣ����е�ȴԶ���ں��ߣ���ԭ����ǰ�ߵķ��Ӽ������� | |
| C�� | CO2��SiO2�����ۻ�ʱ�����˷��������������ͬ | |
| D�� | ������Ԫ������aXm+��bYn-������ͬ�ĵ��Ӳ�ṹ����a��b |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 2SO3��
2SO3���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| �����Լ� | ���� | |
| ���飨��ϩ�� | ��ˮ | ϴ�� |
| �����ƾ��� | ˮ | ��Һ |
| �ֱ�������ᴿ | ˮ | �ؽᾧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������̫���ܵ�صij��ò��� | |
| B�� | NO��SiO2��SO3����ͨ�����Ϸ�Ӧ���� | |
| C�� | ʵ���ҿ���NaOH��Һ����Cl2��SO2���� | |
| D�� | ʵ���ҿ��ù����Ȼ��Ƹ��ﰱ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �٢� | C�� | �ۢ� | D�� | �ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
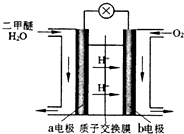 �����ѣ�CH3OCH3����һ����ࡢ��Ч�����������Ļ������ܵĿ�ȼ�����Ϊ21���͵�������Դ����ҵ�Ʊ������ѵ������������£�
�����ѣ�CH3OCH3����һ����ࡢ��Ч�����������Ļ������ܵĿ�ȼ�����Ϊ21���͵�������Դ����ҵ�Ʊ������ѵ������������£��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com