
【题目】(1)在第三周期元素及其单质和化合物中,原子半径最小的元素是________(用元素符号或化学式表示,下同);氧化性最强的单质是________;还原性最强的单质是________;最高价氧化物对应的水化物中酸性最强的是________;碱性最强的是________;形成的两性氢氧化物是________。
(2)在某温度下,于密闭容器中进行下列反应:2SO2(气)+O2(气)![]() 2SO3(气)起始:c(SO2)=3mol/L,c(O2)=2mol/L,达平衡时,80%的SO2转化为SO3,这时c(SO2)=________mol/L,c(O2)=________mol/L,c(SO3)=________mol/L
2SO3(气)起始:c(SO2)=3mol/L,c(O2)=2mol/L,达平衡时,80%的SO2转化为SO3,这时c(SO2)=________mol/L,c(O2)=________mol/L,c(SO3)=________mol/L
(3)燃烧11.2L(标准状况)甲烷,生成二氧化碳的物质的量为________,生成水的质量为________。
【答案】Cl Cl2 Na HClO4 NaOH Al(OH)3 0.6 0.8 2.4 0.5mol 18g
【解析】
同周期除0族元素外,从左到右,原子半径逐渐减小,单质氧化性逐渐增强、还原性逐渐减弱,最高价氧化物对应水合物酸性逐渐增强、碱性逐渐减弱。
(1)综上分析,在第三周期元素及其单质和化合物中,原子半径最小的元素是Cl;氧化性最强的单质是Cl2;还原性最强的单质是Na;Cl元素的最高价氧化物对应的水化物酸性最强,化学式为HClO4;Na元素的最高价氧化物对应的水化物碱性最强,化学式为NaOH;第三周期中Al(OH)3为两性氢氧化物。
(2) 在某温度下,于密闭容器中进行下列反应:2SO2(气)+O2(气)![]() 2SO3(气)起始:c(SO2)=3mol/L,c(O2)=2mol/L,达平衡时,80%的SO2转化为SO3,则SO2反应了的浓度为80%
2SO3(气)起始:c(SO2)=3mol/L,c(O2)=2mol/L,达平衡时,80%的SO2转化为SO3,则SO2反应了的浓度为80%![]() 3mol/L=2.4 mol/L,氧气反应的浓度为1.2 mol/L,生成的三氧化硫的浓度为2.4 mol/L,故此时c(SO2)=(3-2.4)mol/L =0.6mol/L,c(O2)=(2-1.2) mol/L=0.8mol/L,c(SO3)=2.4mol/L。
3mol/L=2.4 mol/L,氧气反应的浓度为1.2 mol/L,生成的三氧化硫的浓度为2.4 mol/L,故此时c(SO2)=(3-2.4)mol/L =0.6mol/L,c(O2)=(2-1.2) mol/L=0.8mol/L,c(SO3)=2.4mol/L。
(3) 11.2L(标准状况)甲烷的物质的量为![]() ,根据甲烷的分子式CH4可知,生成二氧化碳的物质的量为0.5mol,生成水的质量为
,根据甲烷的分子式CH4可知,生成二氧化碳的物质的量为0.5mol,生成水的质量为![]() 。
。


科目:高中化学 来源: 题型:
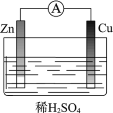
【题目】某原电池装置如图所示。其中,Zn电极为原电池的______极(填“正”或“负”),电极反应式是______________。Cu电极上发生的反应属于______(填“氧化”或“还原”) 反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】头孢拉定又名先锋霉素,是常用的一种抗生素,其结构简式如下:
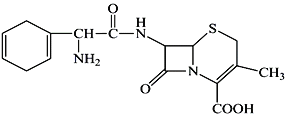
下列说法不正确的是 ( )
A. 头孢拉定的分子式是C16H19N3O4S,分子中有多种官能团
B. 头孢拉定与Na2CO3溶液、NaHCO3溶液都可以反应
C. 头孢拉定既可与盐酸反应,也可与NaOH溶液反应
D. 1mol头孢拉定最多可与5mol H2和3mol Br2发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下,超氧化钾晶体(KO2)呈立方体结构。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则下列有关说法正确的是( )

A. KO2中只存在离子键
B. 超氧化钾的化学式为KO2,每个晶胞含有1个K+和1个O2-
C. 晶体中与每个K+距离最近的O2-有6个
D. 晶体中,所有原子之间都以离子键相结合
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中属于加成反应的是( )
A. CH4+Cl2![]() CH3Cl+HCl
CH3Cl+HCl
B. CH2===CH2+HCl―→CH3CH2Cl
C. CH3CH2OH+HBr![]() CH3CH2Br+H2O
CH3CH2Br+H2O
D. 2CH3CH3+7O2![]() 4CO2+6H2O
4CO2+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是合成药物盐酸沙格雷酯的重要中间体,其合成路线如图:
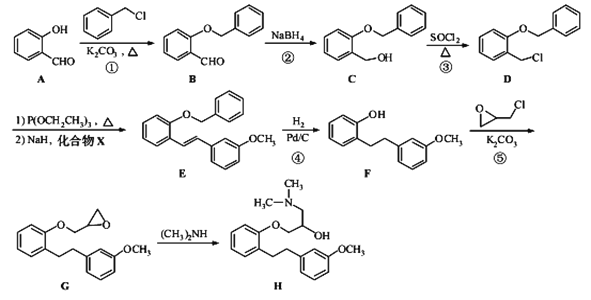
(1)化合物A中的含氧官能团为___和___(填官能团名称)。
(2)反应⑤的反应类型是___,反应方程式___。
(3)B的分子式___,1molB与足量的银氨溶液反应,最多能产生___gAg。
(4)检验D中卤原子种类,所需的试剂有___。
(5)写出同时满足下列条件的B的一种同分异构体的结构简式:___。
a.分子中含有两个苯环;
b.分子中有7种不同化学环境的氢;
c.不能与FeCl3溶液发生显色反应,但水解产物之一能发生此反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数由小到大排列的四种短周期元素X、Y、Z、W的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。M元素与X同主族,与W同周期。
(1)M元素是________(填元素符号)。
(2)Z、W形成的气态氢化物的稳定性为________>________。(填化学式)
(3)写出M2Z2的电子式:________,写出M2Z2与水反应的离子方程式: _____________。
(4)由X、Y、Z、W四种元素中的三种组成一种强酸,该强酸的稀溶液能与铜反应,离子方程式为______。
(5)由X、Y、Z、W四种元素组成一种离子化合物A,已知:①1 mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体。②A能与盐酸反应产生气体B,该气体能与氯水反应。则A是________(填化学式)。写出气体B与氯水反应的离子方程式:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】立方烷(C8H8)外观为有光泽的晶体。其八个碳原子对称地排列在立方体的八个角上。以下相关说法错误的是
A. 立方烷在空气中可燃,燃烧有黑烟产生
B. 立方烷一氧代物1种、二氯代物有3种、三氯代物也有3种
C. 立方烷是苯(C6H6)的同系物、也是苯乙烯(C6H5-CH=CH2)的同分异构体
D. 八硝基立方烷完全分解可能只产生二氧化碳和氮气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com