
分析 (1)固体粒子之间的相互作用力很大,把粒子紧扣在一起,所以粒子只能在固定的位置上振动;
(2)含有自由移动离子或电子的物质能导电;
(3)在熔融状态下或水溶液里能导电的化合物是电解质;
(4)在水溶液里和熔融状态下都不导电的化合物是非电解质.
解答 解:(1)组成物质的微粒之间存在相互作用,各微粒之间既有相互吸引力,又有相互排斥力,当微粒距离较近时,排斥力的作用明显,将微粒推开,当微粒距离较大时,吸引力的作用明显,将微粒拉近,所以通常微粒在较平衡的位置上做极小的运动,即只能在各自平衡位置附近做微小振动,故选①④;
(2)含有自由移动离子或电子的物质能导电,③铜中含有自由的电子,所以能导电,⑥KNO3溶液、⑦熔融的氢氧化钠 中含有自由移动的离子,所以能导电,故选③⑥⑦;
(3)①食盐晶体、⑤纯醋酸、⑦熔融的氢氧化钠、⑧液态氯化氢 溶于水都能导电,且都是化合物,所以都是电解质,故选①⑤⑦⑧;
(4)②乙醇和④蔗糖在水溶液里或熔融状态下都以分子存在,所以都是非电解质,故选②④.
点评 本题考查电解质和非电解质的判断、能导电的物质等知识点,注意电解质不一定导电,导电的不一定是电解质.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:填空题
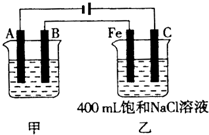 如图为相互串联的甲、乙两电解池.试回答:
如图为相互串联的甲、乙两电解池.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol | B. | 0.2 mol | C. | 0.3mol | D. | 0.4 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胶体和溶液均能通过滤纸 | |
| B. | 胶体加入某些盐可产生沉淀,而溶液不能 | |
| C. | 胶体是一种介稳性的分散系,而溶液是一种非常稳定的分散系 | |
| D. | 胶体能够发生丁达尔现象,而溶液则不能 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)亚磷酸(H3PO3)是二元酸,与足量NaOH溶液反应,生成Na2HPO3,电解Na2HPO3溶液可得到亚磷酸,装置示意图如下:
(1)亚磷酸(H3PO3)是二元酸,与足量NaOH溶液反应,生成Na2HPO3,电解Na2HPO3溶液可得到亚磷酸,装置示意图如下:查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | “白毛”的主要咸分是氧化铝 | |
| B. | 在长出“白毛”过程中,铝片的温度会升高 | |
| C. | 若用硝酸汞溶液代替汞就无法看到类似的现象 | |
| D. | 此过程中涉及到的化学变化与原电池的原理有关 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com