
在密闭容器中,对于反应:2SO2(g)+O2(g)⇌2SO3(g),SO2和O2起始时分别为20mol和10mol;达平衡时,SO2的转化率为80%.若从SO3开始进行反应,在相同的温度下,欲使平衡时各成分的百分含量与前者相同,则起始时SO3的物质的量及其转化率为()
A. 10 mol和10% B. 20 mol和20% C. 20 mol和40% D. 20 mol和80%
考点: 化学平衡的计算.
专题: 计算题;化学平衡专题.
分析: 在相同的温度下,使平衡时各成分的百分含量相同,说明两平衡是等效平衡,按化学计量转化到一边,对应成分的物质的量相同,据此计算从SO3开始进行反应,达相同的平衡状态,需要SO3的物质的量;
根据从SO2和O2起始达平衡时,SO2的转化率为80%SO2,据此计算平衡时n(SO3),从SO3开始进行反应,达相同的平衡状态,SO3的物质的量相同,SO3的起始物质的量减去平衡时物质的量为转化的SO3的物质的量,据此计算转化率.
解答: 解:在相同的温度下,使平衡时各成分的百分含量相同,说明两平衡是等效平衡,按化学计量转化到一边,对应成分的物质的量相同,根据方程式2SO2(g)+O2(g)⇌2SO3(g)可知,20molSO2和10molO2完全转化,可得n(SO3)=n(SO2)=20mol,故从SO3开始进行反应,达相同的平衡状态,需要SO3的物质的量为20mol;
从SO2和O2起始达平衡时,SO2的转化率为80%SO2,转化的n(SO2)=20mol×80%=16mol,由硫元素守恒可知据平衡时n(SO3)=n(SO2)=16mol,所以从SO3开始进行反应,达相同的平衡状态,SO3的物质的量相同为16mol,转化的SO3的物质的量为20mol﹣16mol=4mol,SO3转化率为 ×100%=20%.
×100%=20%.
故选B.
点评: 本题考查化学平衡计算、等效平衡等,难度中等,清楚等效平衡规律是解题的关键.


 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案科目:高中化学 来源: 题型:
下列关于“焰色反应”的理解正确的是( )
|
| A. | 只有金属单质才有焰色反应 |
|
| B. | 只有金属化合物才有焰色反应 |
|
| C. | 只有某些金属或其化合物才有焰色反应 |
|
| D. | 只有金属离子才有焰色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
填空
(1) 可命名为 .
可命名为 .
(2)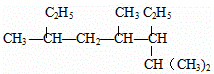 的系统命名为 .
的系统命名为 .
(3)2.5﹣二甲基﹣2,4﹣己二烯的结构简式:
(4)相对分子质量为72且沸点最低的烷烃的结构简式为: .
查看答案和解析>>
科目:高中化学 来源: 题型:
pH=a的某电解质溶液中,插入两支惰性电极通直流电一段时间后,溶液的pH>a,则该电解质可能是()
A. Na2SO4 B. H2SO4 C. AgNO3 D. NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
在一支注射器中,装有NO2和N2O4(无色)的混合气体,它们的相互转化关系为:2NO2(g)⇌N2O4(g).在达到平衡状态后,如果慢慢压缩气体使体积变为原来的二分之一,此时混合气体的颜色与原来相比()
A. 由红棕色变为无色 B. 变浅
C. 由无色变为红棕色 D. 变深
查看答案和解析>>
科目:高中化学 来源: 题型:
下列两个热化学方程式:2H2(g)+O2(g)═2H2O(l)△H=﹣571.6kJ/mol;C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=2 220kJ/mol.现有H2和C3H8的混合气体共5mol,完全燃烧时放热3 847kJ,则在混合气体中H2和C3H8的体积比是()
A. 2:1 B. 3:1 C. 4:1 D. 5:1
查看答案和解析>>
科目:高中化学 来源: 题型:
铜合金是人类使用最早的金属材料,铜在化合物中的常见化合价有+l、+2.已知Cu2O与稀硫酸反应,溶液呈蓝色.现向Cu、Cu2O和CuO组成的混合物中,加入1L 0.6mol/L HNO3溶液恰好使混合物溶解,同时收集到2240mL NO气体(标准状况).请回答下列问题:
(1)写出Cu2O跟稀硝酸反应的离子方程式
(2)若将上述混合物用足量的H2加热还原,所得到固体的质量为 .
(3)若混合物中含0.1mol Cu,将该混合物与稀硫酸充分反应,至少消耗H2SO4的物质的量为 .
(4)若混合物中Cu的物质的量为n mol,则n的取值范围为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com