
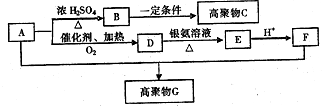
 ÓŠ»śĪļA³£ÓĆ×÷ÓŠ»śŗĻ³ÉµÄÖŠ¼äĢ壮15.2gøĆÓŠ»śĪļČ¼ÉÕÉś³É26.4gCO2ŗĶ14.4gH2O£»ÖŹĘ×Ķ¼±ķĆ÷ĘäĻą¶Ō·Ö×ÓÖŹĮæĪŖ76£¬ŗģĶā¹āĘ×·ÖĪö±ķĆ÷A·Ö×ÓÖŠŗ¬ÓŠO-H¼üŗĶC-O¼ü£®ŗĖ“Ź²ÕńĒāĘ×ÉĻÓŠČżøö·å£¬·åĆ껿֮±ČĪŖ2£ŗ1£ŗ1£®AÄÜ·¢ÉśČēĶ¼×Ŗ»Æ£ŗ
ÓŠ»śĪļA³£ÓĆ×÷ÓŠ»śŗĻ³ÉµÄÖŠ¼äĢ壮15.2gøĆÓŠ»śĪļČ¼ÉÕÉś³É26.4gCO2ŗĶ14.4gH2O£»ÖŹĘ×Ķ¼±ķĆ÷ĘäĻą¶Ō·Ö×ÓÖŹĮæĪŖ76£¬ŗģĶā¹āĘ×·ÖĪö±ķĆ÷A·Ö×ÓÖŠŗ¬ÓŠO-H¼üŗĶC-O¼ü£®ŗĖ“Ź²ÕńĒāĘ×ÉĻÓŠČżøö·å£¬·åĆ껿֮±ČĪŖ2£ŗ1£ŗ1£®AÄÜ·¢ÉśČēĶ¼×Ŗ»Æ£ŗ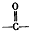 £¬ŌņHµÄ½į¹¹¼ņŹ½æÉÄÜĪŖCH3CH2CHO”¢
£¬ŌņHµÄ½į¹¹¼ņŹ½æÉÄÜĪŖCH3CH2CHO”¢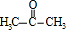 £®
£®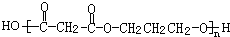 +£Ø2n-1£©H2O£®
+£Ø2n-1£©H2O£® ·ÖĪö 26.4gCO2ĪŖ$\frac{26.4g}{44g/mol}$=0.6mol£¬14.4gH2OĪŖ$\frac{14.4g}{18g/mol}$=0.8mol£¬15.2gAÖŠŃõŌŖĖŲÖŹĮæĪŖ15.2g-0.6mol”Į12g/mol-0.8mol”Į2”Į1g/mol=6.4g£¬n£ØO£©=$\frac{6.4g}{16g/mol}$=0.4mol£¬15.2gAµÄĪļÖŹµÄĮæĪŖ$\frac{15.2g}{76g/mol}$=0.2mol£¬ÓŠ»śĪļÖŠN£ØC£©=$\frac{0.6mol}{0.2mol}$=3£¬N£ØH£©=$\frac{0.8mol”Į2}{0.2mol}$8£¬N£ØO£©=$\frac{0.4mol}{0.2mol}$=2£¬¹ŹAµÄ·Ö×ÓŹ½ĪŖC3H8O2£®ŗģĶā¹āĘ×·ÖĪö±ķĆ÷A·Ö×ÓÖŠŗ¬ÓŠO-H¼üŗĶC-O¼ü£¬ŗĖ“Ź²ÕńĒāĘ×ÉĻÓŠČżøö·å£¬·åĆ껿֮±ČĪŖ2£ŗ1£ŗ1£¬ŌņAĪŖHOCH2CH2CH2OH£¬AµÄĻą¶Ō·Ö×ÓÖŹĮæ±ČBµÄĻą¶Ō·Ö×ÓÖŹĮæ“ó18£¬·¢ÉśĶŃĖ®·“Ó¦£¬ĒŅBæÉŅŌ·¢Éś¼Ó¾Ū·“Ó¦£¬¹ŹA·¢ÉśĻūČ„·“Ӧɜ³ÉB£¬ŌņBĪŖCH2=CHCH2OH£¬CĪŖ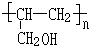 £®A·¢Éś“ß»ÆŃõ»ÆÉś³ÉDĪŖOHCCH2CHO£¬DÓėŅų°±ČÜŅŗ·“Ӧɜ³ÉEĪŖNH4OOCCH2COONH4£¬EĖį»ÆµĆµ½FĪŖHOOCCH2COOH£¬AÓėFĖõ¾Ū·“Ӧɜ³ÉGĪŖ
£®A·¢Éś“ß»ÆŃõ»ÆÉś³ÉDĪŖOHCCH2CHO£¬DÓėŅų°±ČÜŅŗ·“Ӧɜ³ÉEĪŖNH4OOCCH2COONH4£¬EĖį»ÆµĆµ½FĪŖHOOCCH2COOH£¬AÓėFĖõ¾Ū·“Ӧɜ³ÉGĪŖ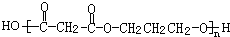 £®
£®
½ā“š ½ā£ŗ26.4gCO2ĪŖ$\frac{26.4g}{44g/mol}$=0.6mol£¬14.4gH2OĪŖ$\frac{14.4g}{18g/mol}$=0.8mol£¬15.2gAÖŠŃõŌŖĖŲÖŹĮæĪŖ15.2g-0.6mol”Į12g/mol-0.8mol”Į2”Į1g/mol=6.4g£¬n£ØO£©=$\frac{6.4g}{16g/mol}$=0.4mol£¬15.2gAµÄĪļÖŹµÄĮæĪŖ$\frac{15.2g}{76g/mol}$=0.2mol£¬ÓŠ»śĪļÖŠN£ØC£©=$\frac{0.6mol}{0.2mol}$=3£¬N£ØH£©=$\frac{0.8mol”Į2}{0.2mol}$8£¬N£ØO£©=$\frac{0.4mol}{0.2mol}$=2£¬¹ŹAµÄ·Ö×ÓŹ½ĪŖC3H8O2£®ŗģĶā¹āĘ×·ÖĪö±ķĆ÷A·Ö×ÓÖŠŗ¬ÓŠO-H¼üŗĶC-O¼ü£¬ŗĖ“Ź²ÕńĒāĘ×ÉĻÓŠČżøö·å£¬·åĆ껿֮±ČĪŖ2£ŗ1£ŗ1£¬ŌņAĪŖHOCH2CH2CH2OH£¬AµÄĻą¶Ō·Ö×ÓÖŹĮæ±ČBµÄĻą¶Ō·Ö×ÓÖŹĮæ“ó18£¬·¢ÉśĶŃĖ®·“Ó¦£¬ĒŅBæÉŅŌ·¢Éś¼Ó¾Ū·“Ó¦£¬¹ŹA·¢ÉśĻūČ„·“Ӧɜ³ÉB£¬ŌņBĪŖCH2=CHCH2OH£¬CĪŖ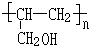 £®A·¢Éś“ß»ÆŃõ»ÆÉś³ÉDĪŖOHCCH2CHO£¬DÓėŅų°±ČÜŅŗ·“Ӧɜ³ÉEĪŖNH4OOCCH2COONH4£¬EĖį»ÆµĆµ½FĪŖHOOCCH2COOH£¬AÓėFĖõ¾Ū·“Ӧɜ³ÉGĪŖ
£®A·¢Éś“ß»ÆŃõ»ÆÉś³ÉDĪŖOHCCH2CHO£¬DÓėŅų°±ČÜŅŗ·“Ӧɜ³ÉEĪŖNH4OOCCH2COONH4£¬EĖį»ÆµĆµ½FĪŖHOOCCH2COOH£¬AÓėFĖõ¾Ū·“Ӧɜ³ÉGĪŖ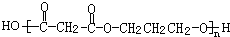 £®
£®
£Ø1£©AµÄ·Ö×ÓŹ½ŹĒC3H8O2£¬ÓŠ»śĪļBĪŖCH2=CHCH2OH£¬ŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘŹĒ£ŗōĒ»ł£¬
¹Ź“š°øĪŖ£ŗC3H8O2£»ōĒ»ł£»
£Ø2£©D”śEµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗOHCCH2CHO+4Ag£ØNH4£©2OH$\stackrel{”÷}{”ś}$NH4OOCCH2COONH4+4Ag”ż+6NH3+2H2O£¬
¹Ź“š°øĪŖ£ŗOHCCH2CHO+4Ag£ØNH4£©2OH$\stackrel{”÷}{”ś}$NH4OOCCH2COONH4+4Ag”ż+6NH3+2H2O£»
£Ø3£©CH2=CHCH2OHµÄĶ¬·ÖŅģ¹¹ĢåHŗ¬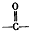 £¬ŌņHµÄ½į¹¹¼ņŹ½æÉÄÜĪŖCH3CH2CHO”¢
£¬ŌņHµÄ½į¹¹¼ņŹ½æÉÄÜĪŖCH3CH2CHO”¢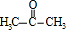 £¬
£¬
¹Ź“š°øĪŖ£ŗCH3CH2CHO”¢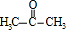 £»
£»
£Ø4£©A+F”śGµÄ»Æѧ·½³ĢŹ½ĪŖ£ŗn HOCH2CH2CH2OH+n HOOCCH2COOH$”ś_{”÷}^{ÅØĮņĖį}$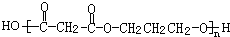 +£Ø2n-1£©H2O£¬
+£Ø2n-1£©H2O£¬
¹Ź“š°øĪŖ£ŗn HOCH2CH2CH2OH+n HOOCCH2COOH$”ś_{”÷}^{ÅØĮņĖį}$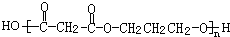 +£Ø2n-1£©H2O£®
+£Ø2n-1£©H2O£®
µćĘĄ ±¾Ģāæ¼²éÓŠ»śĪļĶʶĻ£¬¹Ų¼üŹĒ¼ĘĖćČ·¶ØAµÄ·Ö×ÓŹ½£¬ŠčŅŖѧɜŹģĮ·ÕĘĪÕ¹ŁÄÜĶŵĊŌÖŹÓė×Ŗ»Æ£¬ŌŁ½įŗĻ·“Ó¦Ģõ¼ž½ųŠŠĶʶĻ£¬ÄѶČÖŠµČ£®


 ÓżӾ«¾ķĻµĮŠ“š°ø
ÓżӾ«¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
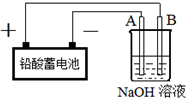 Cu2OŹĒŅ»ÖÖ°ėµ¼Ģå²ÄĮĻ£¬ŹµŃéŹŅÓĆĒ¦ĖįŠīµē³Ųµē½āŅ»¶ØÅØ¶ČµÄNaOHČÜŅŗÖʱøCu2O£¬·½³ĢŹ½ĪŖ2Cu+H2O$\frac{\underline{\;µē½ā\;}}{\;}$Cu2O+H2”ü×°ÖĆČēĶ¼ĖłŹ¾£¬»Ų“šĻĀĮŠĪŹĢā
Cu2OŹĒŅ»ÖÖ°ėµ¼Ģå²ÄĮĻ£¬ŹµŃéŹŅÓĆĒ¦ĖįŠīµē³Ųµē½āŅ»¶ØÅØ¶ČµÄNaOHČÜŅŗÖʱøCu2O£¬·½³ĢŹ½ĪŖ2Cu+H2O$\frac{\underline{\;µē½ā\;}}{\;}$Cu2O+H2”ü×°ÖĆČēĶ¼ĖłŹ¾£¬»Ų“šĻĀĮŠĪŹĢā²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Į½øö·“Ó¦ÖŠ¶¼Ö»ÓŠŅ»ÖÖŌŖĖŲ»ÆŗĻ¼Ū·¢Éśøıä | |
| B£® | Į½øö¹ż³ĢÉś³ÉKClµÄĪļÖŹµÄĮæĻąĶ¬ | |
| C£® | ·¢ÉśŃõ»Æ·“Ó¦µÄŌŖĖŲĻąĶ¬ | |
| D£® | ·¢Éś»¹Ō·“Ó¦µÄŌŖĖŲĻąĶ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1L0.5mol/LNaHCO3ČÜŅŗÖŠHCO3-µÄŹżÄæŠ”ÓŚ0.5 NA | |
| B£® | 1mol-OHŗĶ1molOH-Ėłŗ¬µē×ÓŹżĪŖNA | |
| C£® | 25”ꏱ£¬0.1mol/LKOHČÜŅŗÖŠŗ¬ÓŠOH-µÄŹżÄæĪŖ0.1NA | |
| D£® | 78g±½ÖŠŗ¬ÓŠĢ¼ĖįĖ«¼üµÄŹżÄæĪŖ3NA |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
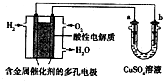
| A£® | Č¼ĮĻµē³Ų¹¤×÷Ź±£¬Õż¼«·“Ó¦ĪŖ£ŗO2+4H++4e-ØT2H2O | |
| B£® | a¼«ŹĒĢś£¬b¼«ŹĒĶŹ±£¬b¼«Öš½„Čܽā£¬a¼«ÉĻÓŠĶĪö³ö | |
| C£® | a¼«ŹĒ“æĶ£¬b¼«ŹĒ“ÖĶŹ±£¬æÉŅŌ“ļµ½ĶµÄ¾«Į¶ÄæµÄ | |
| D£® | a”¢bĮ½¼«¾łŹĒŹÆÄ«Ź±£¬ŌŚĻąĶ¬Ģõ¼žĻĀa¼«²śÉśµÄĘųĢåÓėµē³ŲÖŠĻūŗĵÄH2Ģå»żĻąµČ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | c£ØSO42-£©”Öc£ØCrO42-£© | B£® | c£ØSO42-£©£¾c£ØCrO42-£© | C£® | c£ØSO42-£©£¼c£ØCrO42-£© | D£® | ĪŽ·ØÅŠ¶Ļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Õż·“Ó¦»ī»ÆÄÜŠ”ÓŚ125.4kJ•mol-1 | |
| B£® | Äę·“Ó¦»ī»ÆÄÜŅ»¶ØŠ”ÓŚ125.4kJ•mol-1 | |
| C£® | Äę·“Ó¦»ī»ÆÄܲ»Š”ÓŚ125.4kJ•mol-1 | |
| D£® | Õż·“Ó¦»ī»ÆÄܱČÄę·“Ó¦»ī»ÆÄÜ“ó125.4kJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĢśŗĶĻ”ĻõĖį·“Ó¦ Fe+2H+ØTFe2++H2”ü | |
| B£® | ĀČ»ÆĢśČÜŅŗµĪČė·ŠĖ® Fe3++3H2O $\frac{\underline{\;\;”÷\;\;}}{\;}$ Fe£ØOH£©3”ż+3H+ | |
| C£® | ĻõĖįŅųČÜŅŗÖŠµĪČėŹ³ŃĪĖ® NaCl+Ag+ØTAgCl”ż+Na+ | |
| D£® | ĀČĘųĶØČėÉÕ¼īČÜŅŗ Cl2+2OH-ØTCl-+ClO-+H2O |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com