
A、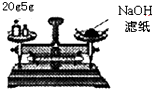 称取固体质量 |
B、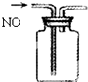 收集NO气体 |
C、 配制溶液 |
D、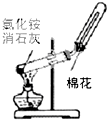 制取氨 |


科目:高中化学 来源: 题型:
A、溴乙烷在氢氧化钠水溶液中加热,该反应的离子方程式:CH3CH2Br+OH-
| |||
B、实验室制乙烯的化学方程式:CH3CH2OH
| |||
C、苯酚钠溶液中通入少量CO2反应的离子方程式: +H2O+CO2→ +H2O+CO2→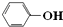 +HCO3- +HCO3- | |||
D、乙醛溶液与足量的银氨溶液共热的离子方程式:CH3CHO+2Ag(NH3)2++2OH-
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 叙述 | 判断 | |
| A | 青苹果汁遇碘水变蓝色 | 青苹果汁中含有葡萄糖 |
| B | 熟苹果汁遇碘水不变蓝色 | 熟苹果中不含淀粉 |
| C | 熟苹果汁可还原银氨溶液 | 熟苹 果汁中只含葡萄糖不含淀粉 |
| D | 熟苹果汁遇碘水变蓝色 | 熟苹果汁中只含淀粉不含葡萄糖 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原电池中电流由负极流向正极 |
| B、原电池中电子流出的一极是正极,发生氧化反应 |
| C、原电池的两极发生的反应均为氧化还原反应 |
| D、形成原电池后,原电池中的阳离子向正极移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、ZnC2水解生成乙烷(C2H6) |
| B、Al4C3水解生成丙烷(C3H4) |
| C、Mg2C3水解生成丙炔(C3H4) |
| D、Li2C2水解生成乙烯(C2H4) |
查看答案和解析>>
科目:高中化学 来源: 题型:
 工业上常将铬镀在其他金属表面,同铁、镍组成各种性质的不锈钢,在如图装置中,观察到图1装置铜电极上产生大量的无色气泡,而图2装置中铜电极上无气体产生,铬电极上产生大量有色气体,则下列叙述正确的是( )
工业上常将铬镀在其他金属表面,同铁、镍组成各种性质的不锈钢,在如图装置中,观察到图1装置铜电极上产生大量的无色气泡,而图2装置中铜电极上无气体产生,铬电极上产生大量有色气体,则下列叙述正确的是( )| A、图1为原电池装置,Cu电极上产生的是O2 |
| B、图2装置中Cu电极上发生的电极反应式为:Cu-2e-═Cu2+ |
| C、由实验现象可知:金属活动性Cu>Cr |
| D、两个装置中,电子均由Cr电极流向Cu电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 普通锌锰干电池构造如图,电池反应为:Zn+2MnO2+2NH4+═2MnO(OH)+2NH3+Zn2+.回答下列问题:
普通锌锰干电池构造如图,电池反应为:Zn+2MnO2+2NH4+═2MnO(OH)+2NH3+Zn2+.回答下列问题: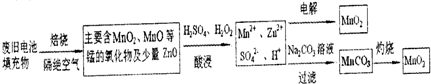
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com