
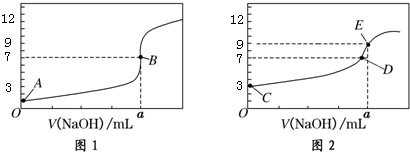
| A. | 图1是滴定CH3COOH 溶液的曲线 | |
| B. | 图2若用甲基橙作指示剂达到滴定终点时,则溶液由黄色变为红色 | |
| C. | 点D所示溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | 如果C、E两点对应的pH分别为3、9,则水电离的氢离子浓度之比为1:100 |
分析 A.图1中0.1000mol/L酸的pH=1,而醋酸为弱酸,0.1000mol/L的醋酸的pH一定>1;
B.用氢氧化钠滴定醋酸,滴定终点时溶液由橙色变为黄色;
C.D点溶液为中性,则c(Na+)=c(CH3COO-)、c(OH-)=c(H+);
D.酸、碱溶液抑制了水的电离,C点中的氢氧根离子、E点中的氢离子是水电离的,据此结合溶液的pH计算出水电离的氢离子浓度之比.
解答 解:A.图1中0.1000mol/L酸的pH=1,说明该酸在溶液中完全电离,为强电解质,而醋酸为弱酸,0.1000mol/L的醋酸的pH一定>1,图1应该为盐酸、图2为醋酸,故A错误;
B.图2为氢氧化钠溶液滴定醋酸,甲基橙变色范围为3.1-4.4,颜色为红、橙、黄,当滴定终点时溶液颜色应该由橙色变为黄色,故B错误;
C.根据图示可知,D点为中性,则c(OH-)=c(H+),结合电荷守恒可知:c(Na+)=c(CH3COO-),溶液中正确的离子浓度大小为:c(Na+)=c(CH3COO-)>c(OH-)=c(H+),故C错误;
D.C点为酸溶液,pH=3的醋酸中,氢离子抑制了水的电离,溶液中氢氧根离子是水电离的,则水电离的氢离子浓度为10-11mol/L,E点为碱性溶液,NaOH过量,氢氧根离子抑制了水的电离,溶液中氢离子是水电离的,则水电离的氢离子浓度为10-9mol/L,故C、E两点水电离的氢离子浓度之比为:10-11mol/L:10-9mol/L=1:100,故D正确;
故选D.
点评 本题考查了酸碱混合的定性判断及溶液pH的计算、离子浓度定性比较等知识,题目难度中等,注意掌握酸碱混合的定性判断方法,明确溶液酸碱性与溶液pH的关系,能够根据电荷守恒、物料守恒及盐的水解原理判断溶液中各离子浓度大小.


科目:高中化学 来源: 题型:选择题
| A. | △H>0、△S>0 | B. | △H<0、△S<0 | C. | △H<0、△S>0 | D. | △H>0、△S<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 植物油不能使溴的四氯化碳溶液褪色( ) | |
| B. | 甲烷和氯气反应生成一氯甲烷与苯和硝酸反应生成硝基苯的反应类型不同 | |
| C. | 乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别 | |
| D. | 苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
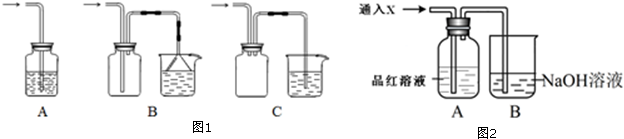
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,0.1 mol•L-1Na2S溶液中存在:c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| B. | 常温下,0.1 mol•L-1HA溶液与0.1 mol•L-1 NaOH溶液正好完全反应时,溶液中一定存在:c(Na+)=c(A-)>c(OH-)=c(H+) | |
| C. | 常温下,pH=7的CH3COONa和CH3COOH混合溶液中c(Na+)=0.1 mol•L-1:c(Na+)=c(CH3COOH)>c(CH3COO-)>c(H+)=c(OH-) | |
| D. | 常温下,向0.1 mol•L-1CH3COOH 溶液加水稀释,当溶液的pH从3.0升到4.0时,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$的值增大到原来的10倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
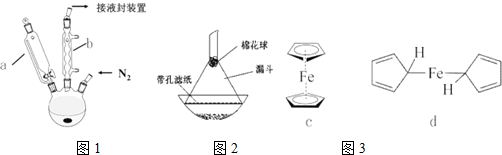
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
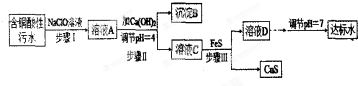
| l离子 | H+ | Cu2+ | Fe3+ | Fe2+ |
| 浓度/(mol•L-1) | 0.1 | 0.05 | 0.04 | 0.002 |
| 物质 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | FeS | CuS |
| Ksp | 4.0×10-22 | 8.0×10-16 | 2.2×10-20 | 6.4×10-12 | 6.0×10-26 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数相同的微粒,它们的化学性质基本相同 | |
| B. | 任何原子的原子核都是由质子和中子构成 | |
| C. | L层上的电子数为奇数的元素一定是主族元素 | |
| D. | 目前使用的长式元素周期表中,最长的周期含36种元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑤ | B. | ①②④ | C. | ③⑤ | D. | 全部正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com