
下列离子方程式表达正确的是( )
A.用惰性电极电解熔融氯化钠:2Cl-+2H2O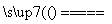 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
B.用氢氧化钠溶液除去铝表面的氧化膜:Al2O3+2OH-===2AlO +H2O
+H2O
C.用稀氢氧化钠溶液吸收二氧化氮:2OH-+2NO2===NO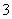 +NO↑+H2O
+NO↑+H2O
D.用食醋除去水瓶中的水垢:CO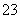 +2CH3COOH===2CH3COO-+CO2↑+H2O
+2CH3COOH===2CH3COO-+CO2↑+H2O
科目:高中化学 来源: 题型:
无色透明溶液中能大量共存的离子组是( )
A.Na+、Al3+、HCO 、NO
、NO
B.AlO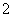 、Cl-、Mg2+、K+
、Cl-、Mg2+、K+
C.NH 、Na+、CH3COO-、NO
、Na+、CH3COO-、NO
D.Na+、NO 、Cl-、I-
、Cl-、I-
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,有浓度均为1 mol·L-1的下列四种溶液:
①H2SO4溶液 ②NaHCO3溶液 ③NH4Cl溶液
④NaOH溶液
(1)这四种溶液pH由大到小的顺序是______,其中由水电离的H+浓度最小的是______。(均填序号)
(2)②中各离子浓度由大到小的顺序是____________,NaHCO3的水解平衡常数Kh=______mol·L-1。(已知碳酸的电离常数K1=4×10-7,K2=5.6×10-11)
(3)向③中通入少量氨气,此时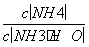 的值______(填“增大”、“减小”或“不变”)。
的值______(填“增大”、“减小”或“不变”)。
(4)若将③和④混合后溶液恰好呈中性,则混合前③的体积______④的体积(填“大于”、“小于”或“等于”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
用如图所示装置分别进行如下实验,测定导电性变化,请按照要求选择填空。
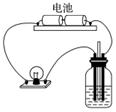
A.导电性变化不大
B.导电性明显增强
C.导电性明显减弱
D.导电性由强到弱再到强
(1)向AgNO3溶液中通入少量HCl( )
(2)向H2SO3溶液中通入Cl2( )
(3)向FeI2溶液中通入少量Cl2( )
(4)向NaOH溶液中通入少量Cl2( )
(5)向NH3·H2O中通入HCl气体( )
(6)向饱和石灰水中不断通入CO2( )
(7)向FeBr2溶液中通入少量Cl2( )
查看答案和解析>>
科目:高中化学 来源: 题型:
离子方程式书写
(1)[2014·新课标全国卷Ⅰ,27(1)]H3PO2是一元中强酸,写出其电离方程式________________________________________________________________________。
(2)[2014·大纲全国卷,27(1)节选]已知非金属元素A最外层电子数与其周期数相同,且A在F中燃烧,产物溶于水得到一种强酸(注:A、F均为短周期元素)。写出一种工业制备单质F的离子方程式
________________________________________________________________________。
(3)[2014·天津理综,9(4)改编]已知Na2S2O3在中性或碱性条件下稳定,在酸性条件下会变黄,用离子方程式表示变黄的原因:________________________________________________________________________。
(4)[2014·山东理综,30(3)节选]取少量铝粉和Fe2O3做铝热反应后所得的固体混合物,将其溶于足量稀H2SO4,滴加KSCN溶液无明显现象,________(填“能”或“不能”)说明固体混合物中无Fe2O3,理由是________________________________________________________________________
(用离子方程式说明)。
(5)[2014·四川理综,8(4)改编]将铜单质的粉末加入NH3的浓溶液中,通入O2,充分反应后溶液呈深蓝色,该反应的离子方程式是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
A.过氧化钠和水反应:2Na2O2+2H2O===4Na++4OH-+O2↑
B.用铜为电极电解饱和食盐水:2Cl-+2H2O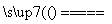 Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C.在明矾溶液中滴加过量氨水:Al3++4NH3·H2O===AlO +4NH
+4NH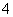 +2H2O
+2H2O
D.向小苏打溶液中加少量Ba(OH)2溶液:HCO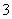 +Ba2++OH-===BaCO3↓+H2O
+Ba2++OH-===BaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下面是以环戊烷为原料制备环戊二烯的合成路线:
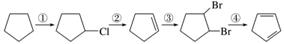
其中,反应①的产物名称是__________,反应②的反应试剂和反应条件是______________,反应③的反应类型是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
NH3、H2S等是极性分子,CO2、BF3、CCl4等是极性键形成的非极性分子。根据上述事实可推出ABn型分子是非极性分子的经验规律是( )
A.分子中不能含有氢原子
B.在ABn分子中A原子的所有价电子都参与成键
C.在ABn分子中每个共价键都相同
D.在ABn分子中A的相对原子质量应小于B的相对原子质量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com