
【题目】第ⅤA族的氮、磷、砷(As)等元素在化合物中常表现出多种氧化态,含第ⅤA族元素的化合物在研究和生产中有许多重要用途。
(1)砷元素的基态原子价电子排布图为______________。
(2)汽车安全气囊的产生药剂主要含有NaN3、Fe2O3、KClO4、NaHCO3等物质,在NaN3固体中阴离子的立体构型______________。
(3)王水溶解黄金的反应如下:Au+HNO3+4HCl=H[AuCl4]+NO↑+2H2O,产物中的H[AuCl4]是配合物,它的配位体是______________,发生电离的方程式为______________
(4)砷化镓属于第三代半导体,它能直接将电能转变为光能,砷化镓灯泡寿命是变通灯泡的100倍,而耗能只有其10%。推广砷化镓等发光二极管(LED)照明是节能减排的有效举措,已知砷化镓的晶胞结构如图,晶胞棱长为apm。
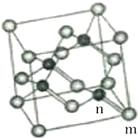
①砷化镓的化学式______________,镓原子的配位数为______________。
②砷化镓的晶胞中m位置Ga原子与n位置As原子之间的距离为________pm (用含“a”的表达式表示)
【答案】(1)![]() ;
;
(2)直线型;
(3)Cl, H[AuCl4] ==="[" AuCl4]-+ H+
(4)①GaAs, 4; ② 。
。
【解析】试题分析:(1)砷元素位于第四周期第ⅤA族,基态原子价电子排布式为4s24p3,基态原子价电子排布图为![]() ,答案为:
,答案为:![]() ;(2)N3-和CO2互为等电子体,分子构型相似,所以N3-的空间构型为直线形,答案为:直线形;(3)H[AuCl4]是配合物,其中H+是外界,[AuCl4]-是内界,中心离子是Au3+,它的配位体是Cl-,发生电离的方程式为H[AuCl4] ==="[" AuCl4]-+ H-+,答案为:ClH[AuCl4] ==="[" AuCl4]-+ H+;(4)①根据砷化镓的晶胞结构图可以看出,As原子主要位于晶胞内,个数为4个,Ga原子位于顶点和面心,个数为8×1/8+6×1/2=4,所以砷化镓的化学式为:GaAs,答案为:GaAs;Ga原子的配位数为4,答案为:GaAs, 4;②砷化镓的晶胞中m位置Ga原子与n位置As原子之间的距离为1/4体对角线的长度,所以距离为
;(2)N3-和CO2互为等电子体,分子构型相似,所以N3-的空间构型为直线形,答案为:直线形;(3)H[AuCl4]是配合物,其中H+是外界,[AuCl4]-是内界,中心离子是Au3+,它的配位体是Cl-,发生电离的方程式为H[AuCl4] ==="[" AuCl4]-+ H-+,答案为:ClH[AuCl4] ==="[" AuCl4]-+ H+;(4)①根据砷化镓的晶胞结构图可以看出,As原子主要位于晶胞内,个数为4个,Ga原子位于顶点和面心,个数为8×1/8+6×1/2=4,所以砷化镓的化学式为:GaAs,答案为:GaAs;Ga原子的配位数为4,答案为:GaAs, 4;②砷化镓的晶胞中m位置Ga原子与n位置As原子之间的距离为1/4体对角线的长度,所以距离为 ,答案为:
,答案为: .
.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】有人设想合成具有下图结构的烃分子。
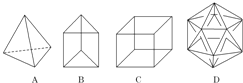
(1)结构D显然是不可能合成的,原因是____________________;
(2)在结构A的每两个碳原子之间插入一个CH2原子团,可以形成金刚烷的结构,金刚烷的分子式为_______;
(3)B的一种同分异构体是最简单的芳香烃,能证明该芳香烃中的化学键不是单双键交替排列的事实是_________;
a.它的对位二元取代物只有一种 b.它的邻位二元取代物只有一种
c.分子中所有碳碳键的键长均相等 d.能发生取代反应和加成反应
(4)C的一种属于芳香烃的同分异构体是生产某塑料的单体,写出合成该塑料的化学方式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯腈(CH2=CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛(CH2=CHCHO)和乙腈(CH3CN)等,回答下列问题:
(1)以丙烯、氨、氧气为原料,在催化剂存在下生成丙烯腈(C3H3N)和副产物丙烯醛(C3H4O)的热化学方程式如下:
①C3H6(g)+NH3(g)+ 3/2O2(g)=C3H3N(g)+3H2O(g) ΔH=-515kJ/mol
①C3H6(g)+ O2(g)=C3H4O(g)+H2O(g) ΔH=-353kJ/mol
两个反应在热力学上趋势均很大,其原因是________;有利于提高丙烯腈平衡产率的反应条件是________;提高丙烯腈反应选择性的关键因素是________。
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应温度为460℃。低于460℃时,丙烯腈的产率________(填“是”或者“不是”)对应温度下的平衡产率,判断理由是________;高于460℃时,丙烯腈产率降低的可能原因是________(双选,填标号)
A.催化剂活性降低 | B.平衡常数变大 | C.副反应增多 | D.反应活化能增大 |
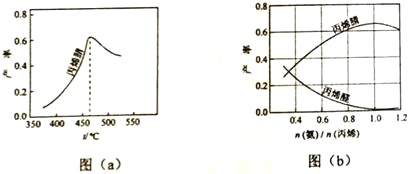
(3)丙烯腈和丙烯醛的产率与n(氨)/n(丙烯)的关系如图(b)所示。由图可知,最佳n(氨)/n(丙烯)约为,理由是_______________。进料氨、空气、丙烯的理论体积约为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳豆是一种减肥食品,从其中分离出一种由C、H、O三种元素组成的有机物A,为确定其结构现进行如下实验:
①相同条件下,测得A的蒸气密度是H2密度的60倍
②6gA在一定条件下完全燃烧,生成3.36L二氧化碳(标况)和1.8g水
③1mol物质A发生酯化反应,转化完全时消耗乙醇92g,等量的A能与足量的金属钠反应放出33.6L氢气(标况)试计算确定: (写过程)
(1)A的分子式____________________
(2)A的结构简式________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,科学家合成了一系列具有独特化学特性的氢铝化合物(AlH3)n。已知,最简单的氢铝化合物的分子式为Al2H6,它的熔点为150℃,燃烧热极高。Al2H6球棍模型如下图。下列有关说法肯定错误的是
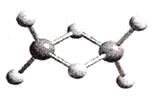
A. Al2H6在固态时所形成的晶体是分子晶体
B. 氢铝化合物可能成为未来的储氢材料和火箭燃料
C. Al2H6中含有离子键和极性共价键
D. Al2H6在空气中完全燃烧,产物为氧化铝和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物A(C10H20O2)具有兰花香味,可用做香皂、洗发香波的芳香赋予剂。
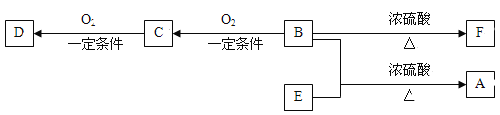
已知:①B分子中没有支链。
②D能与碳酸氢钠溶液反应放出二氧化碳。
③D、E互为具有相同官能团的同分异构体。E分子烃基上的氢若被氯原子取代,其一氯代物只有一种。
④F可以使溴的四氯化碳溶液褪色。
(1)B可以发生的反应有 (选填序号)。
a、取代反应 b、消去反应 c、加聚反应 d、氧化反应
(2)C、D、F分子所含的官能团的名称依次是
(3)写出E的结构简式:
(4)写出C→D的化学方程式:
(5)写出B→F的化学方程式:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂。关于维生素P的叙述正确的是:

A.若R为甲基则该物质的分子式可以表示为C16H10O7
B.分子中有三个苯环
C.lmol该化合物与NaOH溶液作用消耗NaOH的物质的量以及与氢气加成所需的氢气的物质的量分别是4 mol、8 mol
D.lmol该化合物最多可与7molBr2完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D、E、F、G、H、M九种物质,其中A为淡黄色粉末,G为黄绿色气体单质,E为无色气体单质,F的水溶液与石灰水混合可得D的溶液,它们之间的相互转化关系如图,其他与题无关的生成物均已略去。请回答下列问题:
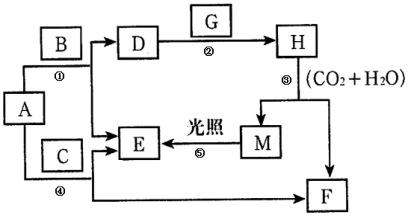
(1)写出H、G的化学式:H ,G 。
(2)写出①、⑤的化学方程式:
① ,⑤ 。
(3)写出③的离子方程式 。
(4)写出F的水溶液与石灰水反应的化学方程式: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com