
硅是重要的半导体材料,构成了现代电子工业的基础。回答下列问题:
(1)基态Si原子中,电子占据的最高能层符号 ,该能层具有的原子轨道数为 、电子数为 。
(2)硅主要以硅酸盐、 等化合物的形式存在于地壳中。
(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以 相结合,其晶胞中共有8个原子,其中在面心位置贡献 个原子。
(4)单质硅可通过甲硅烷(SiH4)分解反应来制备。工业上采用Mg2Si和NH4CI在液氨介质中反应制得SiH4,该反应的化学方程式为 。
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
化学键 | C-C | C-H | C-O | Si-Si | Si-H | Si-O |
键能(KJ/mol) | 356 | 413 | 336 | 226 | 318 | 452 |
①硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是 。
②SiH4的稳定性小于CH4,更易生成氧化物,原因是 。
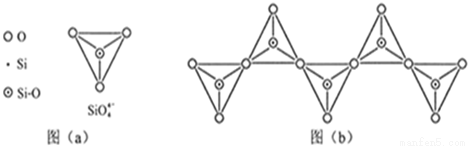
(6)在硅酸盐中,SiO44-四面体(如下图a)通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图b为一种无限长单链结构的多硅酸根;其中Si原子的杂化形式为 。Si与O的原子数之比为 化学式为 。
(1)M;9;4 (2)二氧化硅; (3)共价键;3
(4)Mg2Si+4NH4Cl=SiH4+4NH3+2MgCl2
(5)①硅烷中的Si-Si键和Si-H键的键能小于烷烃分子中C-C键和C-H键的键能,稳定性差,易断裂,导致长链硅烷难以形成,所以硅烷在种类和数量上都远不如烷烃多。
②由于键能越大,物质越稳定,C-H键的键能大于C-O键的键能,故C-H键比C-O键稳定;而Si-H键的键能却远小于Si-O键的键能,所以Si-H键不稳定,而倾向于形成稳定性更强的Si-O键,即更易生成氧化物。
(6)sp3;1:3;[SiO3]n2n-(或SiO32-)
【解析】 (1)基态Si原子中,有14个电子,核外电子排布式为1s22s22p63s23p2,电子占据的最高能层符号为M。该能层具有的原子轨道数为1个s轨道,3个p轨道,5个d轨道。
(2)硅主要以硅酸盐、二氧化硅等化合物的形式存在于地壳中。
(3)单质硅存在与金刚石都属于原子晶体,其中原子与原子之间以共价键相结合,其晶胞中共有8个原子,其中在面心位置贡献为6×1/2=3个原子。
(4)Mg2Si和NH4Cl在液氨介质中反应制得SiH4,该反应的化学方程式为Mg2Si + 4NH4Cl=SiH4+4NH3+2MgCl2。
(5)①硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是①C—C键和C—H键较强,所形成的烷烃稳定。而硅烷中Si—Si键和Si—H键的键能较低,易断裂,导致长链硅烷难以生成。②SiH4的稳定性小于CH4,更易生成氧化物,原因是C—H键的键能大于C—O键,C—H键比C—O键稳定。而Si—H键的键能却远小于Si—O键,所以Si—H键不稳定而倾向于形成稳定性更强的Si—O键。
(6)中心原子Si原子的杂化形式为sp3,Si与O的原子数之比为1∶3,化学式为[SiO3]n2n-(或SiO32-)。


 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源:2014高考名师推荐化学铁及其化合物主要性质(解析版) 题型:选择题
已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示[部分产物略去,Fe能与足量稀HNO3反应生成Fe(NO3)3]。下列说法错误的是
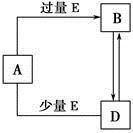
A.A、B、D可能是钠及其化合物
B.A、B、D可能是铁及其化合物
C.A、B、D可能是铝及其化合物
D.A、B、D不可能是非金属及其化合物
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学选做题练习4(解析版) 题型:填空题
避蚊酯(DMP)是一种塑化剂.相对分子质量为194,摄人后对人体有一定的危害,其结构可表示为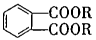 (其中R为烃基)实验室由以下方法可得到DMP
(其中R为烃基)实验室由以下方法可得到DMP
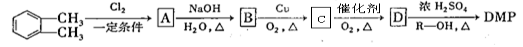
请回答:
(1)物质C中官能团的名称为 。
(2)下列有关DMP的说法可能正确的是 。(填字母标号)
A.DMP的分子式为C10H12O4
B.DMP可以发生取代、加成、氧化等反应
C.DMP在水中的溶解度不大
(3)B与乙二酸(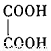 )在一定条件下可以按物质的量1:1发生反应生成高分子化合物,该高分子化合物的结构简式为 。
)在一定条件下可以按物质的量1:1发生反应生成高分子化合物,该高分子化合物的结构简式为 。
(4)工业上以邻二甲苯(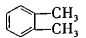 )为原料先生产苯酐(
)为原料先生产苯酐(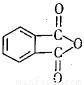 ),再使其与某醇在一定条件下反应制取DMP。苯酐与该醇制取DMP的化学方程式为 。
),再使其与某醇在一定条件下反应制取DMP。苯酐与该醇制取DMP的化学方程式为 。
(5)芳香化合物E与C互为同分异构体,若lmo E与足量银氨溶液反应最多生成2mol Ag,则E可能的结构简式为 。B也存在多种同分异构体,符合下列条件的B的同分异构体有 种。
①l mol有机物可以与2mol NaOH反应
②苯环上的一氯代物只有一种。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学选做题练习2(解析版) 题型:填空题
X、Y、Z、W是元素周期表中原子序数依次增大的四种短周期,其相关信息如下表:
元素 | 相关信息 |
X | X的最高价氧化物对应的水化物化学式为H2XO3 |
Y | Y是地壳中含量最高的元素 |
Z | Z的基态原子最外层电子排布式为3s23p1 |
W | W的一种核素的质量数为28,中子数为14 |
(1)W位于元素周期表第 周期第 族;W的原子半径比X的
(填“大”或“小”)。
(2)Z的第一电离能比W的 (填“大”或“小”);XY2由固态变为气态所需克服的微粒间作用力是 。氢元素、X、Y的原子可共同形成多种分子,写出其中一种能形成同种分子间氢键的物质名称 。
(3)振荡下,向Z单质与盐酸反应后的无色溶液中滴加NaOH溶液直至过量,能观察到的现象是 ;W的单质与氢氟酸反应生成两种无色气体,该反应的化学方程式是 。
(4)在25℃、101kPa下,已知13.5g的Z固体单质在Y2气体中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式是 。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学选做题练习1(解析版) 题型:填空题
聚酰胺—66常用于生产帐篷、渔网、降落伞及弹力丝袜等织物,可利用下列路线合成: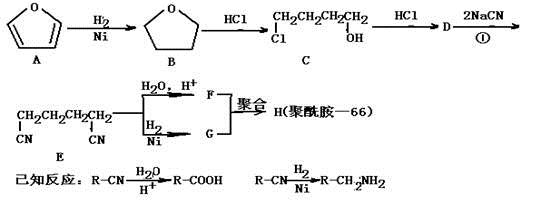
(1)能与银氨溶液反应的B的同分异构体的结构简式为 ,
(2)D的结构简式为 ,①的反应类型为 ,
(3)为检验D中的官能团,所用试剂包括NaOH水溶液及 ,
(4)由F和G生成H的反应方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学资源的综合应用(解析版) 题型:选择题
海水中主要含有Na+、K+、Mg2+、Ca2+、Cl-、Br-、SO42-、HCO3-、CO32-等离子,火力发电时排放的烟气可用海水脱硫,其工艺流程如下图所示,下列说法错误的是

A.海水pH约为8的原因主要是天然海水含CO32-、HCO3-
B.吸收塔中发生的反应有SO2+H2O H2SO3
H2SO3
C.氧化主要是氧气将HSO3-、SO32-、H2SO3氧化为SO42-
D.经稀释“排放”出的废水中,SO42-浓度与海水相同
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学离子方程式的书写及正误判断(解析版) 题型:选择题
下列相关反应的离子方程式书写正确的是
A.氢氧化铁溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O
B.硫酸铜溶液显酸性:Cu2++2H2O=Cu(OH)2↓+2H+
C.向碳酸氢铵溶液中加过量石灰水并加热: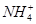 +OH-=NH3↑+H2O
+OH-=NH3↑+H2O
D.用酸化的高锰酸钾溶液氧化双氧水:2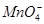 +6H++5H2O2=2Mn2++5O2↑+8H2O
+6H++5H2O2=2Mn2++5O2↑+8H2O
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学碳及其化合物主要性质(解析版) 题型:实验题
生铁中含碳和硫等元素。化学兴趣小组对某生铁样品进行了探究。根据要求回答下列问题。
Ⅰ.生铁中碳和硫元素的定性检验
按如图装置进行实验(夹持仪器已略去,填接口字母代号)可以实现碳和硫元素的检验。
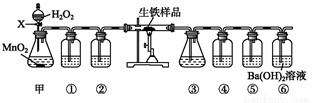
(1)仪器X的名称是 ;装置③⑤中试剂相同,装置④中盛放的试剂是 。(2)写出甲中反应的化学方程式 。(3)如果撤除装置③④⑤,能否确认生铁样品中碳元素的存在? ,理由是 。Ⅱ.生铁中碳、硫质量分数的测定
(4)甲同学认为,以上装置可以粗略测定样品中碳的含量。称取样品w1 g进行实验,充分反应后,测得装置⑥中生成的沉淀为w2 g,该样品中碳的质量分数为 (用含w1、w2的式子表示)。(5)乙同学认为,待一定量样品充分反应后,向装置④中加入过量氯化钡溶液,根据沉淀质量可以计算样品中硫的质量分数,此方案测得的结果 (填“偏大”或“偏小”);若要提高硫元素含量的测定精度,在不改变实验原理的前提下,可以采取的一种措施是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com