
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | K电子数比L层电子数少4个 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |
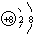 .写出元素Z的气态氢化物的电子式
.写出元素Z的气态氢化物的电子式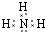 (用元素符号表示)
(用元素符号表示)分析 T单质能与水剧烈反应,所得溶液呈弱酸性,则T为F元素,X的K电子数比L层电子数少4个,核外电子排布为:1S22S22P4,为O元素;第三周期元素的简单离子中半径最小的离子为Al3+,则Y为Al元素;Z的L层有三个未成对电子,核外电子排布为1S22S22P3,为N元素,以此解答该题.
解答 解:T单质能与水剧烈反应,所得溶液呈弱酸性,则T为F元素,X的K电子数比L层电子数少4个,核外电子排布为:1S22S22P4,为O元素;第三周期元素的简单离子中半径最小的离子为Al3+,则Y为Al元素;Z的L层有三个未成对电子,核外电子排布为1S22S22P3,为N元素,
(1)X为O元素,离子核外最外层达到8电子稳定结构,结构示意图为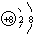 ,Z的氢化物为NH3,电子式为
,Z的氢化物为NH3,电子式为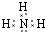 ,
,
故答案为: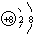 ;
;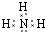 ;
;
(2)Y元素最高价氧化物水化物Al(OH)3,为两性氢氧化物,存在酸式电离和碱性电离两种电离,电离方程式为:H++AlO2-+H2O?Al(OH)3?Al3++3OH-,
故答案为:H++AlO2-+H2O?Al(OH)3?Al3++3OH-;
(3)F的非金属性比Cl元素强,可根据得电子能力判断,氯与F形成的化合物中氯元素呈正价态,说明F易得到电子,则说明F的非金属性强,
故答案为:F;C;
(4)Al为金属元素,具有金属性,其它三种元素为非金属元素,具有较强的非金属性,
故答案为:Al;具有金属性.
点评 本题考查原子结构与元素周期律的关系,题目难度中等,正确推断元素的种类是解答本题的关键,要正确把握元素周期律的递变规律,明确原子结构与元素周期表、元素周期律的关系.


科目:高中化学 来源: 题型:填空题
| 分类依据 | 类别 | 有机化合物序号 |
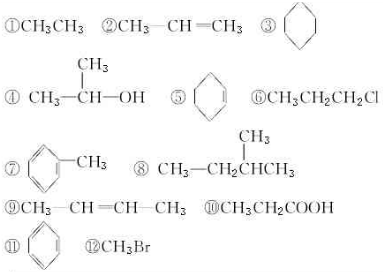
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
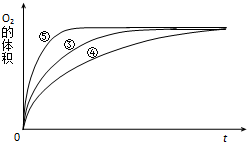 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如下方案完成实验.| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol•L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol•L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol•L-1FeCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 $→_{H_{2}O}^{HCl}$
$→_{H_{2}O}^{HCl}$
 $→_{②Zn/H_{2}O}^{①O_{3}}$
$→_{②Zn/H_{2}O}^{①O_{3}}$
 .
. ;该反应类型酯化反应
;该反应类型酯化反应
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,有机物B与等物质的量的H2发生加成反应可得到有机物A.下列有关说法错误的是( )
,有机物B与等物质的量的H2发生加成反应可得到有机物A.下列有关说法错误的是( )| A. | 有机物A的一氯取代物只有4种 | |
| B. | 用系统命名法命名有机物A,名称为2,2,3-三甲基戊烷 | |
| C. | 有机物A的分子式为C8H18 | |
| D. | B的结构可能有3种,其中一种名称为3,4,4-三甲基-2-戊烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 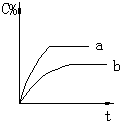 | B. | 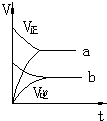 | C. |  | D. | 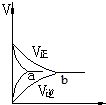 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯使溴水或酸性高锰酸钾褪色均属于加成反应 | |
| B. | 用乙醇与浓硫酸加热至170℃制乙烯的反应属于取代反应 | |
| C. | 用“地沟油”生产生物柴油只发生酯化反应 | |
| D. | 用重铬酸钾溶液检验司机是否酒驾所发生的反应属于乙醇的氧化反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com