
【题目】下列“实验结论”与“实验操作及现象”不相符的一组是
选项 | 试管实验操作及现象 | 实验结论 |
A | 向KI—淀粉溶液中滴加氯水,溶液变成蓝色 | 氧化性:I2>Cl2 |
B | 向蔗糖中滴加浓硫酸,蔗糖变黑 | 浓硫酸有脱水性 |
C | 向某溶液中加入盐酸无现象,再加入BaCl2溶液,有白色沉淀生成 | 溶液中含有 |
D | 向某盐溶液中加入浓氢氧化钠并加热,用湿润的红色石蕊试纸靠近试管口,试纸变蓝 | 溶液中含有 |
A.AB.BC.CD.D
科目:高中化学 来源: 题型:
【题目】聚合物L具有特殊的光学性质,可用于光电材料,其合成路线如下:
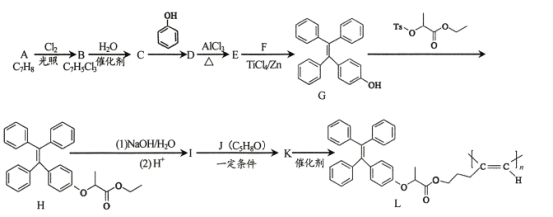
已知:
i.有机物可用键线式表示,如![]() 可表示为
可表示为
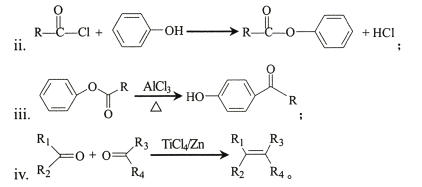
(1) A—B的化学方程式为____。
(2)D的结构简式为____。
(3)E中含有的含氧官能团为____ 。
(4) G—H的反应类型为____。
(5)I—K的化学方程式为____。
(6)下列说法正确的是______填字母序号)。
a.A分子中所有碳原子均在同一平面 b.C的结构简式为![]()
c.F+F—G的副产物中有2种互为顺反异构体 d.1 mol H最多能与2 molNaOH反应
(7)乳酸乙酯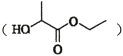 是合成
是合成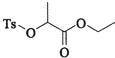 的中间体。下图是某同学设计的合成乳酸乙酯的流程。
的中间体。下图是某同学设计的合成乳酸乙酯的流程。
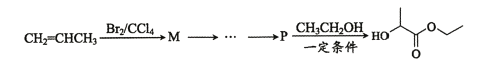
请写出M-P的合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D为石墨电极,E、F分别为短周期相邻的两种活泼金属中的一种,且E能与NaOH溶液反应。按图接通线路,反应一段时间,当电路中通过1.0×10-3mol电子时,下列叙述正确的是( )
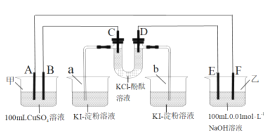
A.U型管中的D端先变红,b烧杯中的溶液会变蓝
B.a烧杯中最多有0.127gI2(KI足量)生成,甲池中的质量会减少0.04g(CuSO4溶液足量)
C.A极产生气体的体积为5.6mL,甲池溶液的pH值为2
D.E电极附近的溶液无明显现象产生
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚氯乙烯是制作装修材料的最常用原料,失火时聚氯乙烯在不同的温度下,发生一系列复杂的化学变化,产生大量有害气体,其过程大体如下:

下列说法不正确的是
A. 聚氯乙烯的单体可由乙烯与HCl加成而得
B. 上述反应中①属于消去反应,④属于(脱氢)氧化反应
C. 火灾中由聚氯乙烯产生的有害气体中含HCl、CO、C6H6等
D. 在火灾现场,可以用湿毛巾捂住口鼻,并弯下腰尽快远离现场
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应的离子方程式书写不正确的是
A.硝酸银溶液与盐酸反应:Ag++HCl=AgCl↓+H+
B.钠与水反应:2Na+2H2O=2Na++2OH-+H2↑
C.氯气与氢氧化钠溶液反应:Cl2+2OH-=Cl-+ClO-+H2O
D.铜与浓硝酸反应:Cu+4H++2![]() =Cu2++2NO2↑+2H2O
=Cu2++2NO2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应NH4Cl+NaNO2![]() NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是
NaCl+N2↑+2H2O放热且产生气体,可用于冬天石油开采。下列表示反应中相关微粒的化学用语正确的是
A. 中子数为18的氯原子:![]()
B. N2的结构式:N=N
C. Na+的结构示意图: 
D. H2O的电子式: ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,利用培养皿探究NH3的性质。实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面。下表中对实验现象所做的解释正确的是( )

选项 | 实验现象 | 解释 |
A | 浓盐酸附近产生白烟 | NH3与浓盐酸反应产生了NH4Cl固体 |
B | 浓硫酸附近无明显现象 | NH3与浓硫酸不发生反应 |
C | 氯化物溶液变浑浊 | 该溶液一定是AlCl3溶液 |
D | 干燥红石蕊试纸不变色,湿润红石蕊试纸变蓝 | NH3是一种可溶性碱 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂,使用过量会使人中毒。某兴趣小组进行下面实验探究,查阅资料知道:① HNO2为弱酸,② 2NO + Na2O2 = 2NaNO2,③ 2NO2 + Na2O2 = 2NaNO3 ④ 酸性KMnO4溶液可将NO和NO2-均氧化为NO3-,MnO4-还原成Mn2+。NaNO2的制备方法可有如下2种方法(夹持装置和加热装置已略,气密性已检验):
制备装置1:
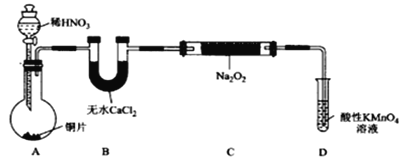
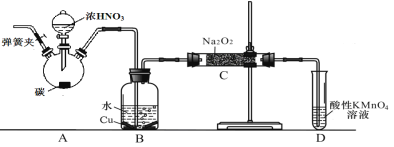
制备装置2:
(1)在制备装置1中:
①如果没有B装置,C中发生的副反应有_________;
②甲同学检查完装置气密性良好后进行实验,发现制得的NaNO2中混有较多的NaNO3杂质;于是在A装置与B装置间增加了_____装置,改进后提高了NaNO2的纯度;
③ D装置发生反应的离子方程式为______。
(2)在制备装置2中:
① B装置的作用是_______________________;
②写出装置A烧瓶中发生反应的化学方程式并用单线桥标出电子的转移___________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫是一种自然界分布较广的元素,在很多化合物中都含有该元素,回答下列问题:
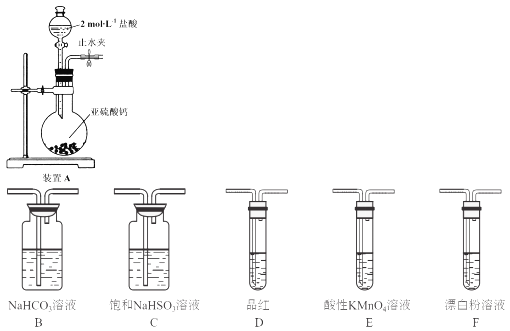
(1)装置A中反应的化学方程式为___________。
(2)使分液漏斗中液体顺利流下的操作是___________。
(3)选用上面的装置和药品探究亚硫酸与次氯酸的酸性强弱:
①甲同学认为按照A→C→F的顺序连接装置即可证明,乙同学认为该方案不合理,其理由是___________。
②丙同学设计的合理实验方案为:A→C→_____→___→D→F,其中装置C的作用是_____,证明亚硫酸的酸性强于次氯酸的实验现象是____。
(4)K2S2O3具有强氧化性,可通过电解H2SO4和K2SO4的混合溶液制得,其阳极反应式为_____。称取0.2500g产品于碘量瓶中,加100mL水溶解,再加入8.000g KI固体(稍过量),振荡使其充分反应;加入适量醋酸溶液酸化,以淀粉为指示剂,用cmol/L的Na2S2O3标准液滴定至终点,消耗Na2S2O3标准液VmL,则样品中K2S2O8的纯度为______%(用含c、V的代数式表示,已知:S2O82-+2I-=2SO42-+I2;2S2O32-+I2=S4O62-+2I-)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com