
| A、不变 | B、先变小后变大 |
| C、逐渐变大 | D、逐渐变小 |
科目:高中化学 来源: 题型:
 在一个容积固定的反应器中,有一可左右滑动的密封隔板,两侧进行如图所示的反应(均加有适量的新型固体催化剂,其体积可忽略不计)
在一个容积固定的反应器中,有一可左右滑动的密封隔板,两侧进行如图所示的反应(均加有适量的新型固体催化剂,其体积可忽略不计)查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、XY |
| B、XY2 |
| C、X2Y |
| D、X2Y3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示原电池装置中,电解质溶液为硫酸,下列有关叙述错误的是( )
如图所示原电池装置中,电解质溶液为硫酸,下列有关叙述错误的是( )| A、锌做负极发生氧化反应 |
| B、供电时的总反应为:Zn+2H+=Zn2++H2 |
| C、该装置可实现化学能转化为电能 |
| D、产生1molH2,消耗锌的质量32.5g |
查看答案和解析>>
科目:高中化学 来源: 题型:
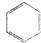 看,分子中含有碳碳双键,由此推测,苯能使酸性高锰酸钾溶液褪色且苯的6个碳原子之间的键有两种.
看,分子中含有碳碳双键,由此推测,苯能使酸性高锰酸钾溶液褪色且苯的6个碳原子之间的键有两种.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com