
| A. | Na+、Ca2+、Cl-、NO3- | B. | Fe2+、H+、SO32-、ClO- | ||
| C. | Mg2+、NH4+、Cl-、SO42- | D. | K+、Fe3+、NO3-、SCN- |
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ③⑤ | C. | ③④ | D. | ②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
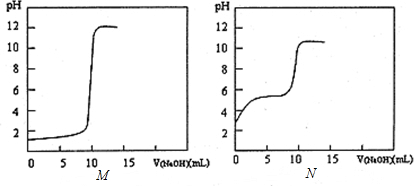
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 方法Ⅰ | 用氨水将SO2转化为(NH4)2SO3、(NH4)2SO4 |
| 方法Ⅱ | 用生石灰吸收SO2,再转化为CaSO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
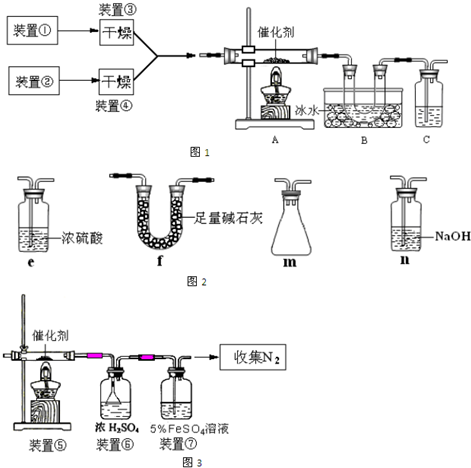
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
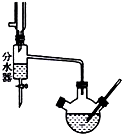 实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表
实验室用乙酸和正丁醇制备乙酸正丁酯.有关物质的相关数据如下表| 化合物 | 相对分子质量 | 密度/g•cm-3 | 沸点/℃ | 溶解度/100g水 |
| 正丁醇 | 74 | 0.80 | 118.0 | 9 |
| 冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
| 乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 有机物 | 试剂 | 现象 |
| ①淀粉 ②苯乙烯 ③苯酚 ④蛋白质 | a.浓硝酸 b.酸性高锰酸钾溶液 c.碘水 d.FeCl3溶液 | A.呈紫色 B.呈蓝色 C.紫色褪去 D.呈黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由石油可以制得汽油 | |
| B. | 乙醇汽油是一种新型的化合物 | |
| C. | 汽车使用乙醇汽油可以减少有害气体的排放 | |
| D. | 由玉米、高梁发酵可以制得乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷在空气中燃烧:CH4+2O2$\stackrel{点燃}{→}$CO2+2H2O | |
| B. | 苯酚钠溶液中通入CO2:C6H5ONa+H2O+CO2$\stackrel{浓硫酸}{→}$C6H5OH+NaHCO3 | |
| C. | 乙醇与浓硫酸在170℃下的反应:2CH3CH2OH$\stackrel{170℃}{→}$CH3CH2OCH2CH3+H2O | |
| D. | 乙酸乙酯和氢氧化钠反应:CH3COOCH2CH3+NaOH$\stackrel{△}{→}$CH3COONa+CH3CH2OH |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com