
在BaSO4饱和溶液中加入少量BaCl2溶液时产生沉淀,若以Ksp表示BaSO4的溶度积常数,则平衡后溶液中( )
A.[Ba2+]=[SO ]=(Ksp)
]=(Ksp)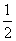
B.[Ba2+]·[SO ]=Ksp,[Ba2+]>[SO
]=Ksp,[Ba2+]>[SO ]
]
C.[Ba2+]·[SO ]>Ksp,[Ba2+]=[SO
]>Ksp,[Ba2+]=[SO ]
]
D.[Ba2+]·[SO ]≠Ksp,[Ba2+]<[SO
]≠Ksp,[Ba2+]<[SO ]
]
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源: 题型:
COCl2(g)  CO(g) + Cl2(g) ΔH > 0,当反应达到平衡时,改变一种反应条件,下列示意图正确的是
CO(g) + Cl2(g) ΔH > 0,当反应达到平衡时,改变一种反应条件,下列示意图正确的是
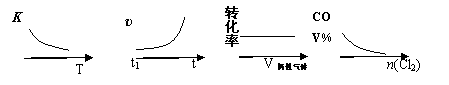
① ② ③ ④
A.①表示随温度升高,平衡常数的变化
B.②表示加入催化剂,反应速率随时间的变化
C.③表示恒压条件下,反应物的转化率随充入惰性气体体积的变化
D.④表示CO的体积分数随充入Cl2量的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
有关麦芽糖的下列叙述中,错误的是( )
①纯净的麦芽糖是无色晶体,易溶于水,有甜味 ②麦芽糖能发生银镜反应,是一种还原性糖 ③1 mol麦芽糖发生水解得到1 mol葡萄糖和1 mol果糖 ④麦芽糖和蔗糖水解的产物完全相同
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
已知难溶电解质在水溶液中存在溶解平衡:
MmAn(s)
 mMn+(aq)+nAm-(aq)
mMn+(aq)+nAm-(aq)
Ksp=[Mn+]m·[Am-]n,称为溶度积。
某学习小组欲探究CaSO4沉淀转化为CaCO3沉淀的可能性,查得如下资料:(25℃)
| 难溶电 解质 | CaCO3 | CaSO4 | MgCO3 | Mg(OH)2 |
| Ksp | 2.8×10-9 mol-2·L-2 | 9.1×10-6 mol-2·L-2 | 6.8×10-6 mol-2·L-2 | 1.8×10-12 mol-3·L-3 |
实验步骤如下:
①往100 mL 0.1 mol·L-1的CaCl2溶液中加入100 mL 0.1 mol·L-1的Na2SO4溶液,立即有白色沉淀生成。
②向上述悬浊液中加入固体Na2CO3 3 g,搅拌,静置,沉淀后弃去上层清液。
③再加入蒸馏水搅拌,静置,沉淀后再弃去上层清液。
④________________________________________________________________________。
(1)由题中信息知Ksp越大,表示电解质的溶解度越______(填“大”或“小”)。
(2)写出第②步发生反应的化学方程式:
________________________________________________________________________
________________________________________________________________________。
(3)设计第③步的目的是
________________________________________________________________________。
(4)请补充第④步操作及发生的现象:
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
物质结构决定性质,深入研究物质的微观结构,有利于理解物质变化的本质。请回答下列问题:
(1)C、Si、N的电负性由大到小的顺序是________;C、N、O、F的第一电离能由大到小的顺序是________。
(2)A、B均为短周期金属元素。依据表中的数据,写出B原子的电子排布式:________。
| 电离能/(kJ·mol-1) | I1 | I2 | I3 | I4 |
| A | 932 | 1 821 | 15 390 | 21 771 |
| B | 738 | 1 451 | 7 733 | 10 540 |
(3)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色。据此判断,[Mn(H2O)6]2+________颜色(填“无”或“有”)。
(4)L的原子核外电子占有9个轨道,而且有一个未成对电子,L是________(填元素符号)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com